
Глава IV. Гломерулонефрит и беременность
Гломерулонефритом болеют 0,1 - 0,2% беременных женщин. Еще полтора - два десятилетия назад допустимость сохранения беременности у женщин, больных гломерулонефритом, ставилась под сомнение и многими врачами даже отвергалась. Основанием для пессимистического прогноза служили высокая перинатальная смертность, частое невынашивание беременности и прогрессирование почечной недостаточности в послеродовом периоде. В дальнейшем тщательное клиническое наблюдение выявило неоднородность патологических состояний у беременных с заболеваниями почек, объединенных под диагнозом "гломерулонефрит". Разнообразие форм этого заболевания определяет в значительной мере течение его во время беременности, частоту акушерских осложнений, а следовательно, и прогноз. Хотя проблема сочетания гломерулонефрита и беременности еще не решена, очевидно, что при определенных формах этого заболевания прогноз можно считать благоприятным, и беременность в таких случаях допустима, в то время как при других формах заболевания беременность представляет опасность для женщины и плода.
Гломерулонефрит - инфекционно-аллергическое заболевание. Возбудителем болезни в большинстве случаев является 12-й тип β-гемолитического стрептококка группы A. Это так называемый нефрогенный штамм стрептококка, чаще всего высеваемый из зева больных острым нефритом. Развитие гломерулонефрита в большинстве случаев связано с перенесенными стрептококковыми заболеваниями (ангина, хронический тонзиллит, острое респираторное заболевание). Нередко источником инфекции являются также стрептококковые кожные заболевания (пиодермия, рожа). Скарлатина, прежде занимавшая ведущее место среди очагов стрептококковой инфекции, отошла в настоящее время на второй план. Рано начатое лечение скарлатины пенициллином значительно сократило частоту возникновения гломерулонефрита после этого заболевания.
Подтверждением стрептококковой этиологии гломерулонефрита служат результаты иммунологического исследования. Стрептококковые антигены находят в крови более чем у половины больных острым гломерулонефритом. Антитела к стрептококковому антигену обнаружены у всех больных острым нефритом. Высота титров анти-О-стрептолизина, антигиалуронидазы и антистрептокиназы служит показателем острого воспалительного процесса в почках. У небольшой части больных возбудителем заболевания является не стрептококк, а стафилококки, пневмококки, дифтерийная пал очка и пр. Возможно также возникновение вакцинного, сывороточного гломерулонефрита, когда белок вакцин или сывороток играет роль антигена.
В развитии гломерулонефрита имеет значение не непосредственный контакт микроорганизма с тканью почки, а иммуноаллергическая реакция организма на инфекцию. Свойственный гломерулонефриту латентный период от перенесенного инфекционного заболевания до появления клинических симптомов нефрита характеризуется снижением сопротивляемости организма, изменением его реактивности, образованием в крови антител к микробам и комплексов антиген - антитело, повреждающих почки, либо аутоантител (комплексы эндогенных антител с белками - антигенами клубочков), ведущих к развитию нефрита. Иммунобиологический процесс длится 2 - 3 нед, прежде чем развиваются гематурия, протеинурия, отеки и гипертония. Время появления клинических признаков заболевания определяется скоростью отложения комплексов антиген - антитело, взаимодействующих с комплиментом, на наружной поверхности базальной мембраны капилляров клубочков под эпителиальными клетками.
Предрасполагает к развитию острого гломерулонефрита охлаждение организма. Однократное резкое охлаждение имеет большее значение для возникновения нефрита, чем привычная работа на холоде. Охлаждение не только способствует активации инфекции, но может играть роль разрешающего фактора в сенсибилизированном организме. Е. М. Тареев (1972) не исключает возможности приобретения белками организма под влиянием охлаждения антигенных свойств. Охлаждение нарушает нормальный кровоток в почке, значительно уменьшая его.
От особенностей реактивности макроорганизма зависит способность образования антител. Этим объясняется меньшая частота заболевания гломерулонефритом у женщин до 30 лет в отличие от мужчин того же возраста, хотя стрептококковые заболевания возникают у тех и других с одинаковой частотой.
Имеются наблюдения, подтвержденные пункционной биопсией почек, свидетельствующие о том, что у некоторых женщин гломерулонефрит впервые возник после перенесенной ранее нефропатии беременных.
Патогенез основных симптомов гломерулонефрита сложен. В происхождении отеков при нефрите принимают участие многие механизмы. Поражение клубочков почек ведет к снижению клубочковой фильтрации. По нашим данным, у беременных, больных гломерулонефритом, клубочковая фильтрация уменьшена на 40% по сравнению со здоровыми беременными и составляет в среднем (при всех формах нефрита) в первом триместре 81,4 мл/мин, во втором - 68,8, в третьем - 64,6, в конце беременности - 61,1 мл/мин. При тех формах гломерулонефрита, которые сопровождаются отеками, клубочковая фильтрация снижается еще больше, и поэтому в организме задерживаются натрий и вода. Канальцевая реабсорбция существенно не изменяется, хотя вне беременности повышение реабсорбции натрия в почечных канальцах играет большую роль в развитии нефритических отеков. Регуляция канальцевой реабсорбции в значительной мере осуществляется альдостероном, а экскреция альдостерона при гломерулонефрите у беременных снижена по сравнению со здоровыми беременными. Так, если у здоровых беременных экскреция альдостерона увеличивается с 20 мкг/сут в первом триместре до 37,2 во втором, до 60,4 в третьем и до 81,5 мкг/сут к концу беременности, то у беременных, больных гломерулонефритом, экскреция альдостерона ко второму триместру достигает только 25 мкг/сут, к третьему - 27,6, а к концу беременности - 39,6 мкг/сут.
В патогенезе отеков имеет значение увеличение проницаемости капилляров для жидкости и белка, вызванное повышением активности гиалуронидазы, деполимеризующей белковомукополисахаридные комплексы межклеточного вещества. О порозности сосудистой стенки можно судить по присутствию белка в отечной жидкости. При нефритах белка в ней содержится до 1%, при сердечных отеках - до 0,3 - 0,5%. Это означает, что при нефритах капиллярная мембрана поражается больше, чем при отеках другого происхождения. Выход в интерстициальное пространство мелкодисперсных фракций белка уменьшает онкотическое давление плазмы крови, что способствует задержке воды в тканях. Этот механизм, образования отеков имеет второстепенное значение при гломерулонефрите у небеременных, однако его роль возрастает во время беременности, когда повышенная порозность стенки капилляров наблюдается даже в физиологических условиях.
Гидратации тканей способствует увеличение содержания в них осмотически активных веществ (соли, мочевина и др.), обусловленное изменениями обмена веществ в тканях и понижением фильтрационной способности почек. При остром нефрите происхождение отеков связано с гиперволемией; при хроническом нефрите гиперволемия отсутствует и большое значение приобретает гиподиспротеинемия.
При нефротических отеках первичным звеном патогенеза является поражение базальной мембраны и эпителиального слоя канальцев почечных клубочков, что приводит к массивной протеинурии. Это ведет к гипопротеинемии, особенно гипоальбуминемии, и к снижению коллоидно-осмотического давления, что нарушает старлинговское равновесие и способствует перемещению жидкости из кровеносного русла в межтканевое пространство с развитием гиповолемии. Транссудация жидкости в ткани происходит также вследствие повышения сосудистой проницаемости за счет активации гиалуронидазы и гипокальциемии, вызванной гиперкальциурией. Гиповолемия рефлекторно раздражает специфические рецепторы и стимулирует секрецию альдостерона. Альдостерон задерживает выделение натрия почками, повышая его реабсорбцию в почечных канальцах. Натрий способствует ретенции связанной с ним воды. Задержка натрия вторично, через реакцию осморецепторов, ведет к усиленной секреции АДГ, что вызывает повышенную ре-абсорбцию воды в дистальных канальцах и накопление жидкости в организме с развитием отеков. Меньшее значение имеет снижение клубочковой фильтрации.
По нашим данным, у больных гломерулонефритом во время беременности отеки появляются чаще, чем вне беременности, причем это не связано с обострением заболевания. Возникновению отеков у беременных, больных гломерулонефритом, способствует общность ряда механизмов, вызывающих отеки при гломерулонефрите и присущих беременности. К ним относятся повышенная проницаемость гематотканевого барьера и выраженное повышение гидрофильности тканевых коллоидов, повышенная активность системы гиалуроновая кислота - гиалуронидаза. Увеличение гидростатического давления в капиллярах, наблюдаещееся при беременности, также способствует возникновению отеков. Снижение клубочковой фильтрации почек во второй половине беременности еще больше ухудшает фильтрационную функцию почек у больных гломерулонефритом и ведет к задержке жидкости в организме. Мы наблюдали отеки у 32% беременных, больных гломерулонефритом. Это были больные острым нефритом, смешанной и нефротической формами хронического гломерулонефрита.
Патогенез артериальной гипертонии при остром гломерулонефрите связан с увеличением объема циркулирующей крови вследствие уменьшения клубочковой фильтрации и ретенции натрия и воды. В результате увеличения притока крови к сердцу возрастает минутный объем крови, при этом периферическое сопротивление кровотоку снижается.
Гемодинамические механизмы гипертонии при хроническом гломерулонефрите иные. По нашим данным, развивается эукинетический (с нормальным сердечным выбросом) или гипокинетический (с уменьшенным минутным объемом крови) тип кровообращения. Периферическое сопротивление кровотоку увеличивается. Если у здоровых беременных удельное периферическое сопротивление в период беременности постепенно уменьшается (в первом триместре - 2320 дин·с·см-5·м2, во втором - до 2070, в третьем - до 1770 дин·с·см-5·м2), то у беременных с гипертонической или смешанной формой хронического гломерулонефрита этот показатель существенно увеличен: в первом триместре - 2700, во втором - 2450, в третьем - 2220 дин·с·см-5·м2.
Среди регуляторных механизмов, обусловливающих изменение гемодинамики при почечной гипертонии, важнейшее место принадлежит системе ренин - ангиотензин - альдостерон и ретенции натрия.
Вне беременности уменьшение почечного кровотока, свойственное гломерулонефриту, ведет к усилению продукции ренина юкстагломерулярным аппаратом почек. Под действием ренина α2-глобулин (ангиотензиноген) превращается в ангиотензин - I, который в свою очередь под влиянием конвертирующего фермента переходит в ангиотензин II. Последний является мощным вазоконстриктором, действующим на стенки сосудов непосредственно или через симпатико-адренергическиё центры продолговатого мозга. Прессорное действие при этом обусловлено не повышением сердечного выброса, а увеличением периферического сопротивления кровотоку за счет сужения артериол. Действуя на эпителий почечных канальцев, ангиотензин задерживает в организме натрий. Другой и более важный путь воздействия ангиотензина на баланс электролитов заключается в стимуляции ангиотензином секреции альдостерона надпочечниками. Альдостерон задерживает экскрецию натрия почечными канальцами; натрий и эквивалентное количество воды накапливаются в сосудистой стенке, делают ее ригидной, уменьшают просвет сосуда и повышают периферическое сопротивление кровотоку. Кроме того, увеличение содержания внутриклеточного натрия повышает чувствительность сосудов к вазоактивным веществам: катехоламинам, ангиотензину и др.
Во время беременности почечный кровоток у больных гломерулонефритом уменьшен. При гипертонической и смешанной формах гломерулонефрита (сопровождающихся повышением артериального давления) он составляет в первом триместре 820 мл/мин, во втором - 780 мл/мин, в третьем - 720 мл/мин, в то время как у здоровых беременных этот показатель соответственно равен 1460; 1150 и 1045 мл/мин. При столь значительном уменьшении почечного кровотока можно было бы ожидать резкого увеличения секреции и активации ренина и альдостерона. Однако, по нашим данным, при гипертонии у беременных, больных гломерулонефритом, активность ренина ниже, чем при физиологической беременности. Таким образом, происходят изменения, прямо противоположные тем, которые наблюдаются при гипертонии вне беременности. Это можно объяснить следующим образом. Во время беременности ренин секретируется не только юкстагломерулярным аппаратом почек, но и плацентой. Артериальная гипертония, нарушая кровообращение в плаценте, уменьшает секрецию ренина, а следовательно, и образование ангиотензина и альдостерона, основным стимулятором которого является ангиотензин.
Не существует во время беременности и "относительного гиперальдостеронизма", обусловленного дефицитом прогестерона - антагониста альдостерона по влиянию на экскрецию натрия почечными канальцами. Нами показано, что содержание прогестерона в крови за время беременности у больных гломерулонефритом увеличивается в 10 раз, т. е. практически в тех же масштабах, как у здоровых беременных (в 9,3 раза), в то время как экскреция альдостерона отстает.
Эти данные не исключают роли системы ренин - ангиотензин - альдостерон в патогенезе артериальной гипертонии у беременных, так как активность ренина и величина экскреции альдостерона при гипертонии у беременных отчетливо выше, чем у небеременных. Кроме того, по данным литературы, при гипертонии у беременных активность ферментов ангиотензиназ, инактивирующих ангиотензин, понижена, а чувствительность к ангиотензину повышена. Последнее может быть обусловлено и увеличением при гипертонии беременных содержания внутриклеточного натрия, что ведет к утолщению сосудистой стенки и более выраженной реакции на воздействие прессорных веществ.
В последние годы появились сообщения о роли депрессорных веществ в генезе артериальной гипертонии у беременных, в частности о значении дефицита кининов и простагландинов A и E. Однако роль депрессорных факторов у беременных с заболеваниями почек практически не изучена. Артериальную гипертонию мы наблюдали у 35% беременных, больных гломерулонефритом. Артериальное давление было повышено при остром нефрите, гипертонической и смешанной формах хронического гломерулонефрита.
Как известно, протеинурия возникает при поражении подоцитов эпителиальных клеток клубочковых капилляров. Количество выделяемого с мочой белка зависит от степени поражения клубочков. Протеинурия такого происхождения обратима и может исчезнуть под влиянием лечения. Поражение эндотелия и базальной мембраны наблюдается при длительном течении заболевания. В таких случаях протеинурия обычно не исчезает.
Почечный фильтр пропускает главным образом низкомолекулярные белки крови с плотностью меньше 70 000 (альбумины). При более глубоком поражении почек в моче появляются и высокомолекулярные белки - глобулины. В последние годы получает распространение изучение селективной протеинурии, т. е. способности поврежденного клубочкового фильтра пропускать белки различной относительной молекулярной массы. Для изучения селективной протеинурии используется метод электрофореза белков мочи. Установлено, что при гломерулонефрите в мочу попадают почти все компоненты сыворотки крови и уропротеинограмма носит название нефротической, или сывороточной. При нефротическом синдроме в моче определяется большое количество альбуминов, α1- и β-глобулины. Содержание α2- и γ-глобулинов увеличено в сыворотке крови, но в моче их нет. Такой тип уропротеинограммы называется нефротическим.
Протеинурию от 0,033 г/л (0,033‰) до 30 г/л (30‰) мы наблюдали у всех беременных, больных гломерулонефритом; особенно высока протеинурия при нефротической форме хронического гломерулонефрита.
Малокровие - одно из частых проявлений патологии почек. Почки участвуют в процессе кроветворения. В них образуется эритропоэтин - гуморальный фактор, регулирующий эритропоэз. Эритропоэтин стимулирует дифференциацию гемоцитобластов костного мозга в сторону эритробластов. Кроме того, эритропоэтин повышает синтез гемоглобина. Анемия при заболеваниях почек нормохромная, реже гипохромная. Таким образом, при болезнях почек развивается своеобразный порочный круг: нарушение эритропоэтической функции почек ведет к развитию анемии, а почки очень чувствительны к гипоксии; снижение количества гемоглобина сопровождается нарушением деятельности канальцев, что усугубляет течение основного заболевания.
При остром гломерулонефрите анемия, помимо нарушения эритропоэза, связана также с разведением крови вследствие гиперволемии, и прежде всего гидремии. Уменьшение концентрации эритроцитов и гемоглобина в единице объема крови происходит и при нормально протекающей беременности, поскольку уже со второго триместра возрастание объема плазмы опережает увеличение количества эритроцитов, при этом показатель гематокрита снижается. По нашим данным, во время физиологической беременности объем плазмы увеличивается на 42%, в то время как объем эритроцитов - только на 20%. В связи с этим показатель гематокрита уменьшается на 11%, развивается умеренная гидремия. Количество эритроцитов уменьшается до 3,5·106 мкл. Содержание гемоглобина снижается до 110 г/л (11 г%). Это обстоятельство следует учитывать, анализируя показатели красной крови у больных гломерулонефри-том. Гиперволемия развивается и у беременных, больных хроническим гломерулонефритом, хотя и не столь значительно, как у здоровых беременных: объем плазмы увеличивается на 26%, объем эритроцитов - на 11%. Об истинной анемии можно говорить при содержании гемоглобина в крови меньше 110 г/л (11 г%) и при показателе гематокрита меньше 33%.
Анемия закономерно наблюдается при хроническом нефрите в стадии почечной недостаточности. При сохранной азотовыделительной функции почек малокровие - нередкое явление, поскольку нарушение продукции эритропрэтина отмечается раньше уремии. Вне беременности анемия при хроническом гломерулонефрите с достаточной азотовыделительной функцией почек встречается у 30 - 40% больных. Среди этих больных во время беременности мы наблюдали малокровие у 26% женщин.
По клиническому течению различают острый и хронический гломерулонефрит. Острый гломерулонефрит чаще принимает циклическую форму, реже встречается ациклическая форма.
Циклическая форма острого гломерулонефрита возникает в среднем через 10 дней (от 1 до 3 нед) после стрептококкового заболевания или вакцинации. Начало заболевания острое: появляются головная боль, боли в пояснице, одышка, отеки на лице, часто отмечается олигурия; повышается артериальное давление; у 1/3 больных развивается лихорадка. С самого начала заболевания выражены изменения мочи: у многих больных легко заметен ее буро-красный цвет, характерный для макрогематурии. Микрогематурия выявляется почти у всех женщин, так же как протеинурия и цилиндрурия. Часто можно обнаружить лейкоцитурию, но при количественном исследовании осадка мочи в ней преобладают эритроциты. Нередко наблюдается умеренная азотемия. Почечная и внепочечная симптоматика заболевания сохраняется от нескольких дней до 2 - 3 нед. Затем постепенно, а иногда довольно быстро увеличивается количество мочи, снижается артериальное давление, исчезают отеки и признаки сердечной недостаточности. Изменения мочи сохраняются долго. Гематурия и протеинурия наблюдаются в течение нескольких месяцев, вплоть до полного выздоровления или перехода заболевания в хроническую форму.
Ациклическая форма острого гломерулонефрита начинается постепенно, незаметно, проявляется маловыраженными отеками на ногах, слабостью, небольшой одышкой и случайно обнаруживаемыми изменениями в моче: протеинурией или гематурией. Болезнь удается диагностировать, если в анемнезе имеются указания на недавно перенесенное стрептококковое заболевание. Титры противострептококковых антитей в этих случаях обычно повышены. Ациклическая форма острого гломерулонефрита чаще, чем циклическая, приобретает хроническое течение.
Во время беременности острый гломерулонефрит встречается редко. Это связано с тем, что заболевание обычно возникает в детском и юношеском возрасте. Кроме того, гиперпродукция глюкокортикоидов, свойственная беременности, по-видимому, препятствует развитию острого гломерулонефрита.
У больных острым гломерулонефритом беременность редко завершается благополучно. У большинства женщин плод погибает внутриутробно или заболевание приводит к преждевременному прерыванию беременности. Оба эти осложнения находятся в тесной зависимости от того, протекает гломерулонефрит с артериальной гипертонией или азотемией. При остром гломерулонефрите без гипертонии и азотемии прогноз более благоприятен.
Острый гломерулонефрит, если он возникает во второй половине беременности, может быть ошибочно принят за поздний токсикоз беременных. Это относится к циклической и в еще большей мере к ациклической форме заболевания. Для дифференциации этих состояний большое значение имеет микроскопическое исследование осадка мочи. Гематурия, кровяные цилиндры свойственны гломерулонефриту и не встречаются при нефропатии беременных. Высокий титр анти-О-стрептолизина также характерен для острого гломерулонефрита. Однако следует иметь в виду, что острый гломерулонефрит может быть нестрептококковой этиологии, тогда титр анти-О-стрептолизина останется низким.
Приводим историю болезни женщины с острым гломерулонефритом.
Больная 28 лет. При сроке беременности 19 нед, через 12 дней после перенесенной ангины, вновь повысилась температура тела, появились олигурия, отеки, артериальное давление поднялось до 180/110 мм рт. ст. В связи с острой почечной недостаточностью применен гемодиализ. Доставлена в клинику при сроке беременности 33 - 34 нед. При поступлении состояние больной тяжелое. Отмечаются одышка, отеки в области поясницы и брюшной стенки; артериальное давление 195/95 мм рт. ст. В моче белок 16,5 г/л (16,5‰), эритроциты и лейкоциты густо покрывают все поля зрения, гиалиновые цилиндры; относительная плотность мочи 1,009. При исследовании мочи по Каковскому - Аддису количество лейкоцитов 8,28·106/сут, эритроцитов 387,54·106 /сут, цилиндров 1,08·106. Клубочковая фильтрация составила 53 мл/мин, канальцевая реабсорбция 99,6%. Анализ крови: эр. 2,7·106 в 1 мкл, Hb 69 г/л (6,9 г%), л. 12,6·103 в 1 мкл; СОЭ 59 мм/ч. Остаточный азот крови увеличился с 0,49 до 1,19 г/л (с 49 до 119 мг%). Мочевина крови 11,3 ммоль (68 мг%). Учитывая тяжесть состояния больной, решено срочно прервать беременность на фоне лечения оксациллином, преднизолоном, фуросемидом (лазиксом), корглюконом, неокомпенсаном, кокарбоксилазой, дибазолом, папаверином, кислородом и витаминами. После вскрытия плодного пузыря плод принял поперечное положение, произошла преждевременная отслойка нормально расположенной плаценты, сопровождавшаяся обильным кровотечением Произведено абдоминальное кесарево сечение. Извлечен мальчик массой 2050 г и длиной тела 46 см в состоянии асфиксии. Ребенок умер через 3 ч. Послеоперационный период осложнился гипокоагуляцией, анемией, двусторонней бронхопневмонией, эндомиометритом. Активный воспалительный процесс в почках продолжался. Остаточный азот и мочевина крови оставались высокими. На 40-й день после операции больная переведена в нефрологическое отделение.
Острый гломерулонефрит, перенесенный за год и более до беременности, после успешно проведенного лечения обычно не предрасполагает к развитию позднего токсикоза беременных, не влияет отрицательно на развитие плода, не оказывает заметного воздействия на последующую функцию почек. Иначе говоря, вылеченный острый нефрит отрицательно не отражается на течении беременности, состояния плода и женщины. В этом мы убедились, наблюдая 18 женщин, переболевших острым гломерулонефритом более чем за год до возникновения беременности. Аналогичные выводы были сделаны и другими исследователями.
Острый гломерулонефрит, не вылеченный в течение года, считают перешедшим в хронический нефрит.
Различают следующие основные формы хронического гломерулонефрита (Е. М. Тареев, 1972): 1) злокачественную (подострая, быстро прогрессирующая); 2) смешанную; 3) нефротическую; 4) гипертоническую; 5) латентную; 6) терминальную.
Подострый злокачественный диффузный гломерулонефрит, в течение 1/2 - 11/2 лет приводящий к гибели больной, по-видимому, развивается у беременных крайне редко. Нам не встретилось ни одного описания такого наблюдения.
При смешанной форме хронического диффузного гломерулонефрита выражены как воспалительно-сосудистые изменения и связанная с ними гипертония, так и дистрофические изменения и связанные с ними протеинурия, гипопротеинемия, гиперхолестеринемия и отеки. Артериальное давление обычно умеренно повышено, тем не менее могут наблюдаться изменения глазного дна, гипертрофия левого желудочка сердца, акцент II тона над аортой. Отеки небольшие и непостоянные. Протеинурия колеблется от следов до 6 г/л (6‰), в осадке мочи обнаруживают различные цилиндры, эритроциты, реже лейкоциты. При смешанной форме хронического гломерулонефрита в одних случаях могут преобладать признаки, характерные для гипертонического нефрита, в других - для нефротического. При этой форме заболевания могут наблюдаться приступы судорог, подобные припадкам эклампсии. Продолжительность жизни больных смешанной формой гломерулонефрита в среднем 5 лет.
Приводим описание сочетания беременности и смешанной формы хронического гломерулонефрита.
Больная 36 лет. С детства болеет хроническим отитом. С 1970 г. отмечалась протеинурия 0,33 - 0,66 г/л (0,33 - 0,66‰). На V мес первой беременности, в 1972 г., повысилось артериальное давление до 180/110 мм рт. ст., содержание белка в моче увеличилось до 6 - 9 г/л (6 - 9‰). На 31-й неделе беременности плод погиб внутриутробно. После родов артериальное давление оставалось повышенным. В октябре 1972 г. и в ноябре 1973 г. обследовалась и лечилась в нефрологическом отделении клиники терапии и профессиональных заболеваний 1-го МММ, где диагностирован хронический гломерулонефрит. Переведена во ВНИИАГ в декабре 1973 г. при второй беременности 22 нед в удовлетворительном состоянии. Артериальное давление 130/70 мм рт. ст., отеков нет. В моче белок 0,29 г/л (0,29‰), относительная плотность мочи 1,007 - 1,020. Проба Нечипоренко: эритроцитов 250, лейкоцитов 750. Общий белок крови 78 г/л (7,8 г%), остаточный азот 0,21 г/л (21 мг%). Клубочковая фильтрация 59,2 мл/мин, канальцевая реабсорбция 99%. При сроке беременности 32 нед поступила в институт повторно в связи с ухудшением состояния (появились признаки позднего токсикоза). Артериальное давление 170/100 мм рт. ст., протеинурия увеличилась до 1,32 г/л (1,32‰); появились отеки. Лечение несколько улучшило состояние больной, но при беременности 35 нед начались роды, осложнившиеся преждевременной отслойкой нормально расположенной плаценты и внутриутробной гибелью плода.
Данный пример демонстрирует осложненное течение как первой, так и второй беременности у женщины со смешанной формой хронического гломерулонефрита. Каждый раз к основному заболеванию присоединялся поздний токсикоз беременных и плод погибал анте- или интранатально.
Нефротическая форма хронического диффузного гломерулонефрита (старое название нефрозонефрит) характеризуется тетрадой симптомов: массивные отеки, выраженная протеинурия, гипопротеинемия и гиперхолестеринемия. Протеинурия может достигать 30 г/л (30‰) и более, в сутки выделяется больше 5 г белка. Вследствие этого развивается гипопротеинемия до 50 - 40 г/л (5 - 4 г%). Атрофируется мускулатура, больные жалуются на прогрессирующую слабость. Гипопротеинемические отеки появляются на ногах, затем на лице, туловище, возникает асцит; в наиболее тяжелых случаях наблюдаются отеки легких, мозга с судорогами и отек сетчатки глаз со слепотой. Больные жалуются на тошноту, отсутствие аппетита. Эти явления обусловлены отеком слизистой оболочки желудка. Резко уменьшается диурез. Из крови в мочу переходят преимущественно альбумины, а1- и в-глобулины. В осадке мочи находят гиалиновые и зернистые цилиндры. Диспротеинемия выражается в нарастании фракций а2- и у-глобулинов. Содержание холестерина в крови достигает 7,8 - 15,6 - 26,0 ммоль/л (300 - 600 - 1000 мг%). Артериальное давление остается нормальным.
Для нефротической формы хронического диффузного гломерулонефрита, помимо дистрофических изменений, характерны также признаки воспалительного поражения почек, выражающиеся в скудной гематурии и уменьшенной клубочковой фильтрации. Почечная недостаточность у больных нефротической формой хронического гломерулонефрита наступает вследствие тяжелого поражения всего нефрона, в особенности канальцев. Увеличение азотистых веществ в крови появляется в тех случаях, когда функция почек понижается на 50% и более.
Течение нефротического синдрома во время беременности, как правило, благоприятное. В литературе описано немногим более 70 больных, 5 больных наблюдали мы. Мнение исследователей в отношении этих больных единодушно: беременность не способствует прогрессированию или обострению заболевания. Скорее наоборот, во время беременности происходит некоторое улучшение состояния больных, по-видимому, под влиянием увеличения эндогенных оксикортикостероидов. Не происходит ухудшения состояния и в послеродовом периоде. Наблюдаемые у некоторых беременных усиление протеинурии и нарастание отеков могут быть скорригированы терапевтическими мероприятиями. Не величина протенурии, даже очень значительная, определяет неблагоприятный прогноз для беременной с нефротическим синдромом, а появление гипертонии или азотемии. Однако эти синдромы во время беременности обычно не развиваются. С селективной протеинурией, свойственной нефротическому синдрому, кровяное русло покидают иммуноглобулины G и γ, их уровень в крови снижается. Возможно, это имеет определенное значение в появлении инфекционных осложнений, в частности инфекции мочевых путей. Существует мнение, что развитие отеков, снижение объема плазмы и гиперлипидемия создают высокий риск развития тромбоэмболии в родах и послеродовом периоде. Подобные указания следует иметь в виду, хотя мы не наблюдали инфекционных и тромбофлебитических осложнений при нефротической форме гломерулонефрита у беременных, рожениц и родильниц.
Приводим пример сочетания беременности с нефротической формой гломерулонефрита.
Больная 24 лет. В самом начале беременности выявлены обширные отеки, и больная направлена в терапевтическое отделение, где диагностирован хронический гломерулонефрит. Беременность рекомендовано было прервать, но больная категорически отказалась от этого. При сроке беременности 18 нед поступила во ВНИИАГ с массивными отеками липа, рук, живота, ног, поясницы. Артериальное давление 110/70 мм рт. ст. В моче 9,9 г/л (9,9‰) белка, относительная плотность мочи 1,008 - 1,021, выщелоченных эритроцитов 30 - 40 в поле зрения, зернистые цилиндры. Проба Нечипоренко: эритроцитов 106,25·103, лейкоцитов 4,25·103. Анализ крови: эр. 2,7·106 - 3,4·106 в 1 мкл, Hb 77 - 102 г/л (7.7 - 10,2 г%), л. 6,2·103 в 1 мкл; СОЭ 56 мм/ч. Общий белок крови 46 - 63 г/л (4,6 - 6,3 г%), холестерин крови 6,8 - 9,8 ммоль/л (262 - 387 мг%), остаточный азот 0,195 - 0,265 г/л (19,5 - 26,5 мг%). Содержание натрия в сыворотке крови 147 ммоль/л, калия 4,86 ммоль/л, кальция 2,1 ммоль/л (4,2 мэкв/л). Клубочковая фильтрация почек 34 мл/мин, канальцевая реабсорбция 97,2%. Почечный кровоток 454 мл/мин. Диагностированы нефротическая форма хронического гломерулонефрита, анемия. Состояние плода оставалось удовлетворительным. Лечение: трансфузии альбумина (5 раз - 1,25 л), плазмы (4 раза - 1,25 л), крови (6 раз - 1,5 л), гипотиазид, верошпирон, микроволновая терапия на область почек. Отеки значительно уменьшились, протеинурия, гипопротеинемия и анемия стали менее выраженными. При сроке беременности 38 нед произведено кесарево сечение. Родился живой мальчик массой 2800 г, длиной 47 см в удовлетворительном состоянии. Мать и ребенок выписаны через 2 нед.
Данный пример свидетельствует о благополучном завершении беременности у женщины с нефротической формой хронического гломерулонефрита при условии длительного наблюдения и лечения в стационаре.
Гипертоническая форма хронического диффузного гломерулонефрита характеризуется повышением артериального давления и небольшими изменениями в моче: протеинурия, цилиндрурия,гематурия невелики и непостоянны. Эта форма хронического гломерулонефрита отличается длительным медленным развитием (20 - 30 лет). Она появляется часто после ациклического латентного острого гломерулонефрита или в результате перенесенной нефропатии беременных. Больные предъявляют мало жалоб и длительное время сохраняют трудоспособность. Развитие гипертонического синдрома напоминает течение доброкачественной формы гипертонической болезни: артериальное давление длительное время неустойчиво, затем становится стабильным. Чаще в большей мере повышено систолическое давление, оно колеблется в течение суток и обычно не приобретает злокачественного характера, т. е. медленно прогрессирует и не достигает крайне высоких цифр: систолическое редко превышает 200 мм, а диастолическое - 120 мм рт. ст. Постепенно увеличиваются размеры левого желудочка сердца, появляется акцент II тона на аорте. При исследовании глазного дна выявляют сужение артерий, более глубокие изменения сетчатки редки и появляются поздно. Отеков нет. Протеинурия редко превышает 1 г/л (1‰). Цилиндрурия незначительная. Гематурия почти постоянная, число эритроцитов варьирует, но не бывает значительным. Медленное развитие гипертонической формы хронического гломерулонефрита объясняется незначительным поражением канальцев почек. Почечная недостаточность наступает, когда воспалительный процесс приводит к дистрофии большого количества нефронов. Азотемия развивается постепенно, медленно.
Приводим пример сочетания беременности и гипертонической формы хронического гломерулонефрита.
Больная 27 лет. Поступила во ВНИИАГ 23/1Х 1977 г. при сроке беременности 20 нед. В 1969 г. во время первой беременности артериальное давление поднялось до 180/120 мм рт. ст., появились отеки и протеинурия до 10 г/л (10‰). При сроке 30 нед развилась преэклампсия и плод погиб внутриутробно. В 1970 г. - вторая беременность. Она сопровождалась такой же клинической картиной, преэклампсией и рождением мертвого плода при сроке беременности 32 нед. После родоразрешения артериальное давление оставалось повышенным, в 1972 г. составляло 260/120 мм рт. ст. и практически не поддавалось лечению. В 1973 г. произошел самопроизвольный аборт при сроке беременности 10 нед. В 1975 г. госпитализирована в Институт кардиологии АМН СССР, где произвели пункционную биопсию почки: диагностирован мембранозно-пролиферативный хронический гломерулонефрит. Выявлены увеличение левого желудочка сердца, клубочковая фильтрация составила 116 мл/мин. Артериальное давление удалось снизить со 180/120 до 140/90 мм рт. ст. Выписана с клиническим диагнозом: гипертоническая форма хронического гломерулонефрита с сохранной функцией почек. Настоящая беременность четвертая. С IV месяца состояние больной ухудшилось. Вновь повысилось артериальное давление, которое не удавалось снизить назначением дибазола, папаверина, гемитона, допегита. Поступила с жалобами на головную боль, одышку при физической нагрузке. Отеков не было. Граница сердца расширена влево до среднеключичной линии. На верхушке сердца выслушивался дующий систолический шум, акцент II тона на аорте. Артериальное давление 170/100 мм рт. ст. В моче белок 0,23 - 1,98 г/л (0,23 - 1,98‰). Относительная плотность мочи 1,022, лейкоцитов 8 - 10 в поле зрения, эритроциты единичные выщелоченные, цилиндры гиалиновые и зернистые единичные. Анализ крови: Hb 112 г/л (11,2 г%), л.6,8-103 в 1 мкл; СОЭ 43 мм/ч. На глазном дне сужение артерий сетчатки. Остаточный азот крови составил 0,27 г/л (27 мг%), мочевина крови 5,66 ммоль/л (34 мг%), общий белок крови 63 г/л (6,3 г%), холестерин крови 4,37 ммоль/л (168 мг%), клубочковая фильтрация почек 58,4 мл/мин, канальцевая реабсорбция 98,8%. Плод погиб внутриутробно на 2-й день после госпитализации женщины.
В данном примере неблагополучное течение всех четырех беременностей. Тяжелый поздний токсикоз, осложнивший первую беременность, привел к гибели плода и вызвал развитие гломерулонефрита. Гипертоническая форма заболевания послужила причиной невынашивания и антенатальной смерти плодов при всех последующих беременностях.
Латентная форма хронического диффузного гломерулонефрита характеризуется только скудным мочевым синдромом (небольшая протеинурия). Цилиндры и эритроциты в моче встречаются редко. Для уточнения особенностей мочевого осадка большое значение приобретают исследования его по Каковскому - Аддису или Нечипоренко. Больные обычно хорошо себя чувствуют и долгое время могут не знать о том, что они больны. Латентная форма хронического нефрита может продолжаться 10 - 20 лет и более и либо перейти в гипертоническую или нефротическую формы, либо сразу завершиться развитием почечной недостаточности. Латентная форма болезни встречается чаще других форм гломерулонефрита как вне, так и во время беременности.
Приводим пример сочетания беременности и латентной формы хронического гломерулонефрита.
Больная 35 лет. В возрасте 3 лет после скарлатины перенесла острый гломерулонефрит. В дальнейшем на протяжении многих лет наблюдался мочевой синдром: протеинурия, микрогематурия. Отеков, повышения артериального давления не было. При обследовании в терапевтическом стационаре диагностирован хронический гломерулонефрит. Настоящая беременность седьмая. В 20 лет благополучно доносила беременность и родила живого ребенка. Затем было 5 искусственных абортов. Поступила во ВНИИАГ при сроке беременности 11 нед. Отеков нет. Артериальное давление 100/60 мм рт. ст. Анализ мочи: белка 0,06 г/л (0,06‰), относительная плотность мочи 1,013 - 1,122, лейкоцитов - 3 - 4 в поле зрения, эритроцитов нет. Проба Нечипоренко: эритроцитов 103, лейкоцитов 0,25·103. Общий анализ крови без особенностей. Остаточный азот крови 0,29 г/л (29 мг%), общий белок крови 80 г/л (8 г%) Клубочковая фильтрация 100 мл/мин, канальцевая реабсорбция 99,5%. Почечный кровоток 1240 мл/мин. Диагностирована латентная форма хронического гломерулонефрита, и беременность признано возможным сохранить. В дальнейшем осложнений в период беременности не было, наблюдалась амбулаторно. Своевременно родился мальчик массой 3600 г, длиной 52 см, в хорошем состоянии.
К латентной форме гломерулонефрита относится гематурический нефрит, характеризующийся стойкой гематурией, незначительной протеинурией и отсутствием внепочечных симптомов заболевания. Эту форму гломерулонефрита нужно тщательно дифференцировать от урологических заболеваний почек и мочевых путей.
Терминальная форма хронического диффузного гломерулонефрита - это конечная стадия нефрита (хроническая уремия). Все формы хронического гломерулонефрита в конце концов переходят в терминальную. Во время беременности эта форма заболевания практически не наблюдается, так как детородная функция резко снижается при значительном поражении почечной паренхимы.
Частота различных форм хронического нефрита у беременных не соответствует таковой вне беременности. Наблюдавшиеся нами беременные, больные хроническим гломерулонефритом, распределялись по формам заболевания следующим образом: латентная у 63% женщин, смешанная у 25%, гипертоническая у 1%, нефротическая у 5%. Большинство беременных страдали наиболее легкой формой заболевания.
Во время обострений хронического гломерулонефрита развивается клиническая картина, подобная острому нефриту, или только усиливается выраженность основных проявлений заболевания: нарастают отеки, увеличиваются протеинурия или гематурия, повышается артериальное давление, растет титр противострептококковых антител.
Обострение хронического гломерулонефрита во время беременности отмечается редко. Мы наблюдали обострение хронического нефрита у трех женщин. У больной с латентной формой хронического гломерулонефрита обострение было диагностировано при сроке беременности 16 нед, когда протеинурия достигла 6,6 г/л (6,6‰), артериальное давление - 160/100 мм рт. ст., появилась анасарка. В 28 нед произошла внутриутробная смерть плода. У другой больной, со смешанной формой гломерулонефрита, обострение воспалительного процесса возникло при сроке 8 нед и беременность была прервана. Обострение заболевания у третьей больной выявлено в 36 нед; досрочно произведено кесарево сечение.
У большинства наблюдавшихся нами женщин, у которых не было обострения гломерулонефрита, симптоматика заболевания была такой же, как до беременности. Основные симптомы гломерулонефрита встречались со следующей частотой: у 35% больных заболевание протекало во время беременности с гипертонией, у 32% - с отеками. У 12% больных гипертонической или смешанной формой нефрита выявлен спазм сосудов сетчатки глаз, а у 21% женщин имелись электрокардиографические признаки изменения миокарда. Акцент II тона во втором межреберье справа у грудины выслушивался у 18% больных с повышенным артериальным давлением.
Протеинурия разной степени - от 0,33 до 30 г/л (от 0,33 до 30‰) наблюдалась у 84% больных. У остальных женщин в моче были только следы белка. Гематурия (от 20 до 100 эритроцитов в поле зрения) отмечена у 46% женщин, цилиндрурия - у 57%. Концентрационная пособность почек была нарушена только у 13,2% больных. Азотемия отмечена у 4 больных. У 65% женщин пробы Нечипоренко или Каковского - Аддиса выявили преобладание гематурии над пиурией.
Анемия во время беременности возникла у 26% больных (Hb 83 - 98 г/л, или 8,3 - 9,8Г%). Гипопротеинемия меньше 65 г/л (6,5 г%) обнаружена у 16% больных с большой протеинурией. Гиперхолестеринемия выявлена у 19% женщин.
Редко во время беременности возникает такая форма заболевания, как очаговый гломерулонефрит. Он развивается не после инфекционного заболевания, а во время него. При этом в результате прямого токсико-бактериального воздействия поражается только часть нефронов. Возбудителями очагового нефрита могут быть разнообразные микроорганизмы. Заболевание возникает чаще в детородном возрасте (20 - 30 лет). Клиническая картина характеризуется появлением изменений в моче во время какого-либо инфекционного заболевания (грипп, острое респираторное заболевание, ангина, пневмония, аппендицит, гнойничковое поражение кожи и др.). Гематурия - наиболее частый симптом. Она может сопровождаться небольшой протеинурией, изредка цилиндрурией. Общие симптомы (отеки, гипертония, гипопротеинемия, азотемия, снижение клубочковой фильтрации) обычно не наблюдаются. Боли в пояснице редкие и слабые. Тяжесть процесса определяется основным инфекционным заболеванием или неинфекционной интоксикацией (например, медикаментозной), а не очаговым нефритом.
Очаговый гломерулонефрит может продолжаться до 2 - 3 мес и затем полностью излечивается. Реже развиваются рецидивирующие формы, при которых гематурия появляется вновь при повторных инфекционных заболеваниях или охлаждении тела.
От латентной формы диффузного хронического гломерулонефита очаговый нефрит можно отличить по данным анамнеза (указания на совпадение начала нефрита с инфекцией или интоксикацией). Кроме того, при латентной форме хронического гломерулонефрита иногда наблюдаются минимальные внепочечные проявления: небольшие отеки под глазами, кратковременное повышение артериального давления, снижены клубочковая фильтрация и фильтрационная фракция.
Прогноз при очаговом нефрите благоприятный. Даже рецидивирующие формы обычно полностью излечиваются и не переходят в хронический диффузный гломерулонефрит. Беременность у женщин с очаговым нефритом обычно не осложняется присоединением позднего токсикоза, преждевременными родами или повышенной перинатальной смертностью. Поэтому очаговый нефрит, развившийся во время беременности, не является показанием для ее прерывания.
Гломерулонефрит оказывает неблагоприятное влияние на течение беременности и особенно на состояние плода. Поздний токсикоз беременных развивается почти у половины больных гломерулонефритом. Это осложнение беременности часто возникает раньше обычных сроков (28 нед). Поздний токсикоз, так же как и другие осложнения (преждевременные роды, незрелость плода), находится в прямой зависимости от того, протекает ли гломерулонефрит с повышенным или с нормальным артериальным давлением. Felding (1969) выявил тяжелый поздний токсикоз у 16,3% больных хроническим гломерулонефритом, перинатальная смертность у них была 143% и незрелость плодов - 12,5%. У больных с нормальным артериальным давлением эти показатели были в 4 - 10 раз меньше, чем у больных с гипертонией.
Анализируя течение беременности при гломерулонефрите, мы обнаружили поздний токсикоз у 35% женщин, в том числе нефропатию у 21%, преэклампсию у 2%; перинатальная смертность составила 140‰. Преждевременная отслойка нормально расположенной плаценты наблюдалась у 2% женщин.
Приводим пример тяжелых последствий присоединения позднего токсикоза.
Больная 22 лет. Страдает смешанной формой хронического гломерулонефрита в течение 4 лет. Беременность первая, развивалась нормально. Систематически находилась под врачебным наблюдением. Функция почек была удовлетворительной: протеинурия 1,98 г/л (1,98‰), клубочковая фильтрация 60 мл/мин, канальцевая реабсорбция 99,2%, относительная плотность мочи 1,008 - 1,025. Артериальное давление 130/70 мм рт. ст. Сосуды глазного дна и ЭКГ без особенностей, остаточный азот крови 0,19 г/л (19 мг%). При сроке беременности 38 нед протеинурия достигла 23 г/л (23‰), артериальное давление повысилось до 140/90 мм рт. ст. Произошла преждевременная отслойка нормально расположенной плаценты. Произведено кесарево сечение. Извлечен мертвый плод массой 3100 г, длиной 53 см. К концу операции началось гипофибриногенемическое кровотечение, развился геморрагический шок, Произведена надвлагалищная ампутация матки. Выявлена острая почечная недостаточность [остаточный азот 1,26 г/л (126 мг%)]. Активная терапия временно несколько улучшила состояние, но на 7-й день после операции больная умерла от множественных кровоизлияний во внутренние органы и вещество мозга.
В развитии позднего токсикоза, несомненно, играет роль нарушенное почечное кровообращение. По нашим данным, у больных латентной формой гломерулонефрита нефропатия беременных развивается реже, чем при более тяжелых формах заболевания. Это объясняется меньшим поражением почек и, в частности, менее выраженным нарушением почечной гемодинамики при латентной форме гломерулонефрита. Антенатальная смерть при латентной форме гломерулонефрита отмечается только в случае присоединения позднего токсикоза. Поскольку при латентной форме гломерулонефрита осложнения редки, мы считаем беременность при этом заболевании допустимой.
При гипертонической и смешанной формах гломерулонефрита, кроме глубокого нарушения регионарного почечного кровообращения, наблюдаются выраженные патологические изменения в общей системе кровообращения. По нашим данным, это способствует в 6 раз более частому, чем при латентной форме, развитию позднего токсикоза беременных, нарушению маточно-плацентарного кровообращения, преждевременной отслойке плаценты и в 10 раз более высокой перинатальной смертности. При этих формах гломерулонефрита продолжение беременности нежелательно.
При нефротической форме хронического гломерулонефрита беременность можно допустить, если есть условия для тщательного наблюдения и длительного стационарного лечения больной. Мы разделяем мнение Mampel (1970) о том, что гипертония больше отягощает прогноз для женщины и внутриутробного плода, чем хроническая недостаточность белка. Именно гипертония является основным фактором, ведущим к антенатальной гибели плода. Дефицит белка, хотя и способствует развитию гипотрофии плода, не так опасен для жизни ребенка, как гипертония. У больных нефротической формой гломерулонефрита мы отмечали самое низкое содержание общего белка в крови - до 46 г/л (4,6 г%). Однако все наблюдавшиеся нами женщины с нефротической формой хронического гломерулонефрита родили живых детей, а наблюдение за женщинами в течение нескольких лет после родов не выявило ухудшения заболевания почек в результате беременности. Это соответствует точке зрения других авторов о том, что состояние матери и плода при нефротической форме гломерулонефрита относительно благополучно, а ухудшения течения заболевания после беременности не наблюдается.
Мы выделяем 3 степени риска, определяющие частоту неблагополучного исхода беременности и родов для матери и плода и ориентирующие врача в отношении прогноза или лечебной тактики.
I степень риска минимальная. Осложнения беременности возникают не более чем у 20% женщин. Беременность редко ухудшает течение заболевания, менее чем у 20% больных.
II степень риска выраженная. Экстрагенитальные заболевания часто (от 20 до 50%) вызывают осложнения беременности поздним токсикозом, самопроизвольным абортом, преждевременными родами; часто наблюдается гипотрофия плода; увеличена перинатальная смертность (до 200‰). Течение заболевания может ухудшиться во время беременности или после родов более чем у 20% больных.
III степень риска максимальная. У большинства женщин с экстрагенитальными заболеваниями возникают осложнения беременности (более 50%), редко родятся доношенные дети в удовлетворительном состоянии; перинатальная смертность высокая (более 200‰). Беременность представляет опасность для здоровья и жизни женщины.
У беременных, больных хроническим гломерулонефритом, степень риска зависит от формы заболевания: I степень риска - латентная форма; II степень риска - нефротическая форма; III степень риска - гипертоническая и смешанная формы, азотемия.
К I степени риска относится и очаговый гломерулонефрит.
В табл. 6 представлена частота осложнений беременности при различных формах гломерулонефрита.
Как видно из данных таблицы, при латентной и нефротической формах заболевания осложнения беременности редки. При гипертонической и смешанной формах гломерулонефрита осложнения возникают почти у каждой больной. Все 10 детей родились у больных со II - III степенью риска в состоянии гипотрофии; III степень риска установлена у больных с повышенным артериальным давлением. К III степени риска мы относим и больных гломерулонефритом любой формы с азотемией. Анализ отдаленных результатов свидетельствует о том, что, если почечная недостаточность была во время беременности, она усиливается после родов. При III степени риска беременность женщинам, страдающим гломерулонефритом, противопоказана.
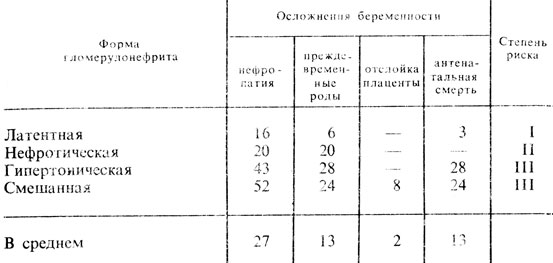
Таблица 6. Осложнения беременности у больных хроническим гломерулонефритом (в процентах)
Следует подчеркнуть, что форма гломерулонефрита определяет прогноз, а не отдельные симптомы заболевания. Dutz (1966) полагает, что благоприятный прогноз возможен только в том случае, если у больной нормальное артериальное давление, клубочковая фильтрация выше 60 мл/мин, относительная плотность мочи более 1,023, нет отеков, протеинурия менее 5 г/сут, легкая гематурия, отсутствуют изменения глазного дна. Мы считаем, что прогноз для беременной и плода благоприятен не только при латентной, но нередко и при нефротической форме.
Больные острым гломерулонефритом в ряде случаев могут доносить беременность до срока родов. Однако при остром гломерулонефрите и обострении хронического нефрита часто возникают внутриутробная смерть плода и преждевременные роды. Заболевание требует длительного интенсивного лечения, которое в ряде случаев небезразлично для плода. В то же время ограничение лекарственных веществ не препятствует переходу болезни в хроническое состояние. Поэтому мы полагаем, что острый гломерулонефрит и обострение хронического нефрита являются противопоказанием к беременности и требуют ее прерывания независимо от срока. Следует при этом помнить, что диагностика обострения хронического нефрита сложна, особенно во время беременности. Ошибка в диагнозе может привести к неоправданному прерыванию беременности (не говоря уже о ненужном лечении). Не каждое ухудшение состояния больной, а также усиление одного или нескольких симптомов являются обострением болезни. Во многих случаях за обострение гломерулонефрита может быть ошибочно принято появление признаков позднего токсикоза беременных. Поэтому необходимо учитывать наличие факторов, которые могли повлечь за собой обострение заболевания (охлаждение, простудные болезни и др.), не упуская из поля зрения, что сама по себе беременность не способствует обострению нефрита. Учитывая стрептококковое происхождение аллергического процесса при нефрите, во многих случаях важное дифференциальное значение может иметь определение титра анти-О-стрептолизина и С-реактивного белка.
Женщины, страдающие хроническим гломерулонефритом, должны быть обследованы в первые 12 нед беременности для уточнения формы заболевания и решения вопроса о сохранении беременности. Наиболее полноценно это может быть сделано в условиях стационара. Поскольку родильный дом располагает меньшими диагностическими возможностями для обследования больных с заболеваниями почек, желательна их госпитализация в терапевтический или специализированный нефрологический стационар.
Больные, у которых установлена латентная форма гломерулонефрита, могут в дальнейшем наблюдаться в женской консультации с целью своевременной диагностики первых признаков обострения хронического гломерулонефрита или позднего токсикоза. Лечить эти патологические состояния следует в стационаре, так как амбулаторное лечение часто менее эффективно и может привести к тяжелым осложнениям. Если обострения гломерулонефрита и позднего токсикоза отсутствуют, то женщины в повторной госпитализации не нуждаются.
Больные нефротической формой гломерулонефрита должны быть госпитализированы столько раз и находиться в стационаре столько времени, сколько требует их состояние (иногда несколько месяцев, вплоть до родов).
Если больные гипертонической и смешанной формами заболевания отказываются от прерывания беременности, на них распространяется тактика, рекомендуемая при нефротической форме. Лечение этих больных в амбулаторных условиях неэффективно, более того, оно даже опасно, так как при отсутствии ежедневного врачебного наблюдения можно своевременно не диагностировать приступ эклампсии, вызванный гломерулонефритом или быстро развивающимся поздним токсикозом.
При латентной форме гломерулонефрита женщины могут рожать своевременно и не нуждаются в каком-либо специальном акушерском пособии. У больных нефротической, смешанной и гипертонической формами болезни нередко развивается гипотрофия плода и, главное, существует угроза его преждевременной внутриутробной смерти. Поэтому не всегда целесообразно дожидаться конца беременности для родоразрешения. В интересах плода бывает показано досрочное возбуждение родовой деятельности, особенно если контроль за состоянием плода, систематически проводимый всеми доступными методами (выслушивание сердцебиения плода, электрофонокардиография плода, определение экскреции эстриола с мочой и уровня термостабильной щелочной фосфатазы в крови и т. д.), начинает указывать на внутриутробное страдание плода или нарушение функции фетоплацентарного комплекса. Кесарево сечение применяется редко, обычно по акушерским показаниям.
Поскольку у больных нефротической, смешанной и гипертонической формами хронического гломерулонефрита может возникнуть необходимость в досрочном родоразрешении, такие женщины должны быть заблаговременно госпитализированы (при сроке беременности 36 - 37 нед). При тех формах болезни, которые протекают с повышенным артериальным давлением (смешанная, гипертоническая), госпитализация за несколько недель до родов определяется не только угрозой для плода, но и состоянием женщины, так как в последние недели беременности артериальное давление часто повышается, что требует соответствующего лечения.
Лечение беременных, больных гломерулонефритом, разработано мало. Между тем оно не может копировать лечение небеременных. Наличие плода выдвигает, с одной стороны, требование обеспечить оптимальные условия для его внутриутробного существования, а с другой - необходимо не нарушить его развития. Это значительно ограничивает проведение необходимых лечебных мероприятий.
Во время беременности женщины соблюдают в основном тот же режим, что и вне ее. Они могут заниматься обычной производственной деятельностью, если она не связана с охлаждением: простудные заболевания могут вызвать обострение гломерулонефрита. Очень желателен такой характер работы, который позволял бы проводить дневной отдых в постели. По данным Г. А. Глезера и Н. П. Москаленко (1974), длительное пребывание в вертикальном положении ухудшает функцию почек (снижаются почечный кровоток, клубочковая фильтрация, диурез, увеличивается протеинурия). Работа предпочтительна сидячая. Если нет обострения заболевания или прогрессирования отдельных его симптомов, необходимость в постельном режиме отпадает. Занятия физкультурой, за исключением комплекса, рекомендуемого беременным женщинам, следует прекратить. Сказанное относится также и к морским купаниям.
Большая роль в лечении гломерулонефрита отводится диете. Основное требование заключается в ограничении поваренной соли и жидкости. Допустимое количество потребления соли зависит от формы заболевания. При остром нефрите содержание поваренной соли в пище не должно превышать 0,3 г в сутки (почти бессолевая диета). По мере ликвидации отеков потребление соли можно несколько увеличить. Если сохраняется значительная гипертония, увеличение поваренной соли не должно быть значительным, потребность в гипонатриевой диете сохраняется.
При остром гломерулонефрите, сопровождающемся олигурией, количество выпитой жидкости и вводимой парентерально должно быть равно диурезу, выделенному накануне, плюс 700 мл жидкости, теряемой внепочечным путем.
При хроническом гломерулонефрите без азотемии также ограничивают потребление поваренной соли, если заболевание протекает с отеками и гипертонией. Потребление соли при нефротической форме нефрита сокращают до 4 - 5 г в сутки, количество выпиваемой жидкости уменьшают до 800 мл. При гипертонической форме хронического гломерулонефрита следует только ограничить прием поваренной соли до 5 г в сутки, при смешанной форме - соли до 5 г, а жидкости до 800 - 1000 мл. В диете при латентной форме хронического гломерулонефрита может содержаться нормальное количество поваренной соли и жидкости.
Сложным и дискуссионным является вопрос о содержании белка в диете больных гломерулонефритом, протекающим без признаков почечной недостаточности. При остром нефрите рекомендуется некоторое ограничение белка: 30 г в сутки в первую неделю заболевания и 50 - 60 г в дальнейшем. Такое сокращение белкового рациона способствует уменьшению выраженности всех основных симптомов болезни, поскольку малобелковая диета снижает работу почек и продукцию антител. Так как беременность у женщин с острым гломерулонефритом должна быть прервана, принцип питания остается тот же, что и при этом заболевании вне беременности.
При лечении хронического гломерулонефрита без азотемии существуют три точки зрения на содержание белка в диете, каждая из них достаточно обоснована. При малобелковой диете (0,5 г/кг) быстрее снижаются отеки и артериальное давление, уменьшается протеинурия. Высокобелковая диета (2 г/кг и более) обеспечивает потребность в белке для покрытия всех пластических затрат, уменьшает гипопротеинемию. Физиологические нормы белка в пище (1 г/кг) - среднебелковая диета переносится легче всего, улучшает состав мочи.
Во время беременности малобелковую диету следует признать неподходящей, так как для роста и развития плода требуется большое количество пластических веществ. С этой точки зрения более оправдана диета, содержащая повышенное количество белка (120 - 160 г в сутки). Она показана при нефротической форме гломерулонефрита, сопровождающейся большой потерей белка с мочой и гипопротеинемией. Следует учесть, что избыток белковых продуктов в пище уже через неделю ухудшает аппетит, усиливает протеинурию, которая может быть в некоторых случаях ошибочно расценена как присоединение нефропатии беременных. При гипертонической и смешанной формах гломерулонефрита рекомендуется диета со средним содержанием белка (70 г в сутки), а при большей потери белка с мочой его дефицит компенсируется парентеральными вливаниями белковосодержащих жидкостей. Диета при латентной форме заболевания не имеет каких-либо особенностей в качественном или количественном составе.
Медикаментозное лечение является основой терапии гломерулонефрита. Однако во время беременности приходится применять только симптоматическое лечение. В этиологической (противострептококковой) терапии нет необходимости, поскольку острый гломерулонефрит во время беременности возникает редко. Патогенетическая терапия гломерулонефрита невозможна, так как используемые для этой цели препараты противопоказаны вследствие эмбриотоксического действия (большие дозы кортикостероидов, цитостатические средства и иммунодепрессанты - имуран и др.). При легком, латентном течении гломерулонефрита беременные вообще не нуждаются в лекарственной терапии.
Лечение почечной симптоматической гипертонии производится теми же средствами, что и лечение гипертонической болезни. В последние годы для этой цели используют следующие основные группы гипотензивных препаратов: 1) производные раувольфии; 2) спазмолитики; 3) салуретики; 4) ганглиоблокаторьц 5) препараты гуанидина; 6) препараты α-метилдофа; 7) клонидин; 8) β-адреноблокаторы; 9) α-адреноблокаторы.
Препараты раувольфии и спазмолитики широко применяются в акушерских учреждениях, однако их эффективность невелика. По данным И. П. Иванова (1969), лечение резерпином, раунатином, дибазолом давало хороший эффект у 37 - 46,5% больных, частичный у 27,7 - 30%, терапевтический эффект отсутствовал у 25,7 - 35% больных.
Препараты раувольфии (резерпин, раунатин, раувазан, серпазил и др.) обладают гипотензивным и седативным (успокаивающим центральную нервную систему) действием. Они способствуют высвобождению норадреналина и предупреждают его депонирование в тканях. Под влиянием препаратов раувольфии уменьшаются запасы норадреналина в стенках артериол и миокарда. Препараты раувольфии снижают как систолическое, так и диастолическое давление, поскольку влияют на адренергические структуры сердца, сосудов, центральной нервной системы. Терапевтический эффект лучше выражен при нестабильной и невысокой гипертонии, действие препарата полностью проявляется на 3 - 5-й день приема, резерпин улучшает почечные функции: увеличиваются почечный кровоток и клубочковая фильтрация.
При лечении препаратами раувольфии могут появиться побочные явления: подавленное настроение, брадикардия, слабость, поносы, боли в области сердца, кожная сыпь. Резерпин и его аналоги не рекомендуется назначать в последние недели беременности, так как они могут способствовать появлению у новорожденных ринита, конъюнктивита, брадикардии, сонливости, угнетению сосательного рефлекса, нарушению дыхания.
Резерпин (рауседил) назначают по 0,1 или 0,25 мг от 1 до 4 раз в сутки в таблетках, индивидуально подбирая оптимальную дозу. Кроме того, рауседил выпускают в ампулах по 1 мл 0,1% раствора (содержащего 1 мг резерпина) и 0,25% раствора (содержащего 2,5 мг резерпина). Вводят рауседил внутримышечно или внутривенно (медленно) 1 - 3 раза в день.
Раунатин обычно действует слабее резерпина, поэтому его назначают 2 - 3 раза в день по 2 таблетки (в 1 таблетке содержится 2 мг препарата).
Из спазмолитических средств с гипотензивной целью применяют дибазол и папаверин. Эти препараты понижают тонус сосудов, оказывая тем самым сосудорасширяющее и гипотензивное действие. Переносятся оба препарата хорошо, побочным эффектом не обладают.
Дибазол назначают внутрь по 0,02 г 3 раза в день или по 2 - 4 мл 1% раствора подкожно, внутримышечно или внутривенно, папаверин - по 0,02 г 3 раза в день, подкожно или внутримышечно по 2 - 4 мл 2% раствора.
Нередко дибазол и папаверин сочетают, назначая их вместе в виде таблеток под названием "папазол" или в инъекциях по 2 мл каждого препарата. Пероральное применение папаверина, дибазола и папазола обычно малоэффективно.
Салуретики, широко используемые в родовспомогательных учреждениях в качестве мочегонных средств, для лечения гипертонии у беременных применяют редко. Между тем они обладают выраженным гипотензивным эффектом. Он обусловлен уменьшением минутного объема крови и снижением периферического сопротивления кровотоку вследствие препятствия реабсорбции натрия в почечных канальцах, потери мышечным слоем и эндотелием сосудов натрия и воды, изменением вне- и внутриклеточных соотношений электролитов и понижением чувствительности сосудов к вазоактивным веществам: катехоламинам, ангиотензину и др. Для длительного лечения гипертонии лучше применять салуретики гипотиазид и гигротон, обладающие продолжительным гипотензивным действием. Фуросемид оказывает быстрое, но непродолжительное гипотензивное действие, поэтому его целесообразно назначать при резком повышении артериального давления, гипертонических кризах. Максимальное гипотензивное действие тиазидных мочегонных средств проявляется не сразу, а через несколько дней, иногда через 2 нед. В некоторых случаях оно не выражено совсем. Поэтому рекомендуется назначать салуретики не изолированно, а в сочетании с каким-либо гипотензивным препаратом. Основным механизмом гипотензивного эффекта диуретиков является уменьшение объема циркулирующей крови. Поэтому салуретики особенно показаны при лечении а-блокаторами, препаратами метилдофы, гуанидина, ганглиоблокаторами. Развитие резистентности к этим препаратам обычно связано с компенсаторной задержкой натрия и воды, т. е. с развитием гиперволемии. В этих случаях снижения артериального давления можно добиться при помощи мочегонных препаратов.
Потенцирующее гипотензивное действие гипотиазида и изобарина заключается в том, что первый выводит из сосудистой стенки натрий и воду, а второй уменьшает тоническое сокращение гладкой мускулатуры сосудов. Комбинированное лечение изобарином и гипотиазидом обосновано еще и потому, что изобарин увеличивает объем плазмы, компенсируя уменьшение объема плазмы, вызванное гипотиазидом. Это особенно важно при лечении больных нефритом, осложненным поздним токсикозом, протекающим с гиповолемией.
Дозы гипотензивных средств при сочетании их с салуретиками могут быть уменьшены в 11/2 - 2 раза. Гипотиазид с гипотензивной целью применяется в дозе 25 - 50 мг 1 раз в день (утром) в течение недели; после перерыва в 3 - 4 дня курс лечения повторяют. Фуросемид назначают по 1/2 таблетки (20 мг) или по 1 таблетке (40 мг) 1 раз в день в течение 3 - 5 дней. Гигротон применяют в таблетках по 100 мг 1 - 4 раза в день; после достижения эффекта дозу уменьшают до 1 таблетки через 1 - 3 дня.
Ганглиоблокаторы, к которым относится большая группа лекарств (бензогексоний, гигроний, пентамин, диколин и др.), тормозят проведение нервных импульсов в симпатических и парасимпатических нервных узлах. Под влиянием ганглиоблокаторов снижается тонус вен. При переходе больной из горизонтального положения в вертикальное кровь скапливается в расширенных венах ног, приток крови к сердцу и сердечный выброс уменьшаются, о ведет к ортостатическому падению артериального давления вплоть до коллапса.
Ганглиоблокаторы могут вызвать разнообразные побочные явления, обусловленные нарушением иннервации внутренних органов: тахикардию, сухость во рту, головокружение, расширение зрачков, нарушение аккомодации, атонию мочевого пузыря и кишечника и т. д. Препараты этой группы противопоказаны при заболеваниях почек и печени. Неблагоприятно влияют ганглиоблокаторы на плод. Имеются сообщения о трансплацентарном переходе ганглиоблокаторов, о тяжелых последствиях для новорожденных вплоть до смерти, возникающих при лечении женщин этими средствами. Описаны частые случаи кишечной непроходимости, повышенной секреции бронхиальных желез, атонии мочевого пузыря у новорожденных.
Мы полагаем, что Ганглиоблокаторы целесообразно использовать только в родах для управляемой гипотонии. С этой целью применяется арфонад. Его вводят внутривенно капельно медленно в виде 0,05 - 0,1% раствора на 5% растворе глюкозы, регулируя количество капель постоянным измерением артериального давления. Действие арфонада наступает очень быстро, и даже незначительная передозировка препарата может вызвать резкое снижение артериального давления и коллапс.
Производное гуанидина - октадин (изобарин, исмелин, санотензин, гуанетидин) является самым сильным из всех известных в настоящее время симпатолитических и гипотензивных средств. Гипотензивное действие октадина связано с его влиянием на уровень и обмен катехоламинов. Симпатолитики вызывают нервно-мышечный блок, препятствуя освобождению ацетилхолина, необходимого для выделения норадреналина нервными окончаниями, и истощают запасы катехоламинов в тканях. Препараты гуанидина имеют большое преимущество перед ганглиоблокаторами, так как они не вызывают блокады парасимпатических ганглиев и таких побочных эффектов как тахикардия, нарушение аккомодации, атония кишечника и мочевого пузыря.
Выраженное симпатолитическое действие октадина целесообразно использовать при лечении беременных, у которых при всех формах гипертонии обнаружено нарушение обмена катехоламинов с преобладанием активности симпатического звена (норадреналина) симпатико-адреналовой системы.
Проведенное нами изучение гемодинамических показателей, изменившихся под влиянием лечения изобарином, показало, что снижение артериального давления связано с нормализацией нарушенного соотношения между величиной сердечного выброса и общим периферическим сопротивлением сосудов. При этом у некоторых больных преимущественно уменьшается сердечный выброс, у других - и минутный объем и общее периферическое сопротивление. Такая особенность гемодинамического действия изобарина представляется очень ценной. Используя изобарин, нам удавалось добиться снижения артериального давления независимо от срока беременности и характера гемодинамических сдвигов, приведших к гипертонии. Отчетливое снижение артериального давления достигнуто у 93,7% больных, причем у 65,5% давление снизилось до нормальных цифр.
Снижение артериального давления под влиянием симпатолитиков сопровождается у некоторых больных уменьшением почечного кровотока и клубочковой фильтрации. Это следует иметь в виду и не назначать продолжительные курсы лечения этим препаратом; обычно достаточно 11 - 12-дневного курса.
Симпатолитики задерживают жидкость в тканях и сосудистом русле. Поэтому их рекомендуется назначать одновременно с мочегонными препаратами (гипотиазид, фуросемид).
Всеми исследователями большое внимание уделяется ортостатическому падению давления, обусловленному действием препаратов гуанидина. В связи с этим рекомендуется начинать лечение с малых доз. Больная должна принимать таблетки лежа в постели и после приема препарата еще в течение 2 ч сохранять горизонтальное положение. Благодаря таким мерам предосторожности мы не отмечали у беременных ортостатического снижения артериального давления, которое могло бы отрицательно сказаться на маточно-плацентарном кровообращении.
Октадин выпускают в таблетках по 25 мг. Назначают по 1/2 таблетки 1 - 2 раза в день, постепенно увеличивая дозу до 2 - 4 таблеток.
Допегит (альдомет) обладает выраженным гипотензивным эффектом и может применяться при стабильной гипертонии. Механизм действия этого препарата связан с нарушением процесса образования адренергического медиатора - норадреналина, который замещается "ложным" медиатором α-метилнорадреналином. Это ослабляет активность симпатических сосудосуживающих влияний. Допегит слабее октадина, но лучше ре носится, ортостатическая гипотония возникает редко и протекает бессимптомно (М. С. Кушаковский, 977). При лечении допегитом клубочковая фильтрация почек не изменяется, так же и почечный кровоток. Побочные явления (депрессия, слабость, сухость во рту). Назначают допегит по 1 таблетке (0,25 г) 1 - 4 раза в день.
Клонидин (гемитон, катапрессан) - производное имидазолина. Обладает центральным (торможение центров симпатической нервной системы в подкорковой области) и периферическим антисимпатикотоническим, а также седативным действием. Гемитон не изменяет содержания катехоламинов в органах и не влияет на их синтез и обмен. Этим он отличается от других гипотензивных средств, уменьшающих активность симпатической нервной системы. Развитие гипотензивного и седативного эффектов сочетается с увеличением концентрации норадреналина в ткани мозга, при этом содержание дофамина и серотонина уменьшается. Экспериментальное изучение механизма действия гемитона свидетельствует о его выраженном центральном влиянии.
По нашим данным, гемитон уменьшает сосудистый тонус, вызывает выраженное уменьшение общего периферического сопротивления кровотоку, а именно этот механизм преобладает при гипертонии у больных гломерулонефритом. Функция почек изменяется в благоприятном направлении: уменьшается сопротивление кровотоку в сосудах почек, несколько увеличивается клубочковая фильтрация. Это может свидетельствовать об избирательном влиянии гемитона на тонус почечных сосудов, что, по-видимому, связано с большой концентрацией препарата в паренхиме почек. Спазмолитический эффект гемитона хорошо выражен; нам удалось добиться снижения артериального давления у 79,2% больных. Побочные явления при лечении гемитоном (тошнота, головокружение) встречаются редко и быстро проходят. Гемитон назначают по 1 таблетке (0,075 мг) 2 - 4 раза в день. Препарат можно вводить подкожно или внутримышечно (в 1 мл раствора содержится 0,15 мг препарата). Внутривенно гемитон вводят медленно после разведения 1 мл препарата в 10 мл изотонического раствора хлорида натрия.
К α-адреноблокаторам относятся фентоламин и тропафен. Фентоламин (регитин) - производное имидазолина, является классическим средством блокады а-адренорецепторов. По характеру действия фентоламин - антагонист адреналина и норадреналина, так как блокирует а-адренореактивные системы, воспринимающие сосудосуживающие импульсы. Установлено, что фентоламин расширяет главным образом мелкие кровеносные сосуды, (артериолы и прекапилляры). Фентоламин менее эффективен во время беременности.
Другой α-адреноб локатор - тропафен оказывает более выраженное и длительное гипотензивное действие. Применяется преимущественно при резком повышении артериального давления (гипертонический криз). Назначают по 1 мл 1% или 2% раствора подкожно или внутримышечно. Препарат хорошо переносится, но может вызвать ортостатическую гипотонию, поэтому больной после инъекции рекомендуется в течение 2 ч сохранять постельный режим.
К наиболее распространенным β-адреноблокаторам относится пропранолол (обзидан, анаприлин, индерал). Он ослабляет влияние симпатической импульсации на β-адренорецепторы сердца, уменьшая минутный объем крови, снижая тем самым артериальное давление. Поскольку β-адреноблокаторы действуют не только на сердечную мышцу, но и на миометрий, способствуя его сокращению, эти препараты во время беременности противопоказаны, так как могут вызвать преждевременное прерывание ее. Применять β-адреноблокаторы во время родов нецелесообразно, поскольку они уменьшают сердечный выброс, который физиологически должен увеличиваться в этот период. Кроме того, гипертония при гломерулонефрите в большинстве случаев связана с повышением периферического сопротивления кровотоку, а не с увеличением минутного объема крови.
Артериальная гипертония быстрее снижается при комбинированном лечении двумя или несколькими препаратами с различным механизмом действия. Такое сочетание позволяет уменьшить дозу каждого препарата без снижения гипотензивного эффекта. Это важно, так как сокращает возможность побочного влияния лекарственных веществ на больную и плод. Широко применяются сочетания препаратов раувольфии с салуретиками; к ним могут быть добавлены симпатолитики, допегит или адреноблокаторы. Выпускаются готовые комбинированные препараты: эрпозид (0,1 мг резерпина и 10 мг гипотиазида), эрпозид-форте (0,25 мг резерпина и 25 мг гипотиазида), адельфан (0,1 мг резерпина и 10 мг непрессола).
При лечении гипертонии у беременных, больных гломерулонефритом, наряду с медикаментозной терапией может применяться физиотерапия. С целью нормализации деятельности вегетативных центров, в частности сосудодвигательного, в комплекс лечебных мероприятий целесообразно включить гальванизацию зоны "воротника" (у больных с эмоциональной неустойчивостью, повышенной раздражительностью, невротическими реакциями) или эндоназальный электрофорез. Оба метода оказывают седативное действие, а гальванизация зоны "воротника" способствует улучшению гемодинамики головного мозга.
Микроволны сантиметрового и дециметрового диапазонов, назначаемые на область почек, вызывают в зоне воздействия расширение сосудов, ускорение кровотока и усиление кровообращения (включая капиллярное), повышение проницаемости капилляров, что способствует усилению в тканях обменных процессов, в том числе окислительно-восстановительных. Определенную положительную роль играет активация функции парасимпатического отдела вегетативной нервной системы. Микроволновая терапия уменьшает сопротивление кровотоку сосудов почек, увеличивает почечный кровоток и тем самым ограничивает влияние ренального механизма гипертонии.
Менее результативна индуктотермия (в виде магнитного поля УВЧ).
Ультразвук на область почек в импульсном режиме излучения обладает выраженным вазотропным влиянием (расширение кровеносных сосудов, изменение скорости кровотока, активация кровообращения), оказывает противовоспалительное десенсибилизирующее действие.
Электроанальгезия обладает отчетливым нейротропным влиянием и способствует регуляции нарушенных корково-подкорковых взаимоотношений, нормализации функционального состояния высших вегетативных центров, в том числе сосудодвигательного. Определенное значение имеет повышение приспособительной способности центральной нервной системы к силе раздражителей, действующих на нее во время беременности.
Физические методы лечения позволяют ограничить дозы гипотензивных средств. Это особенно важно во время беременности, так как возможно неблагоприятное влияние медикаментов на плод.
Для лечения отеков в настоящее время используют различные мочегонные средства. Нет необходимости пользоваться такими слабыми препаратами, как хлорид аммония или ацетат калия, а также ртутными мочегонными средствами (меркузал, новурит, промеран и др.), противопоказанными при всех видах почечных отеков.
Наибольшее распространение в лечении отеков у беременных, в том числе и вызванных гломерулонефритом, получили салуретики, прежде всего диуретики - производные бензотиадиазина (гипотиазид, циклометиазид). Механизм их действия заключается в угнетении реабсорбции натрия в проксимальных отделах канальцев нефрона. Остальные электролиты, кроме калия, выделяются с мочой в значительно меньших количествах, и поэтому происходят небольшие сдвиги в нормальном соотношении электролитов. Диуретическое действие развивается как при ацидозе, так и при алкалозе.
Тиазидовые мочегонные принимают перорально. Они быстро всасываются в организм, их действие начинается через 30 - 60 мин после приема, достигая максимума спустя 2 ч. Продолжительность действия 8 - 12 ч. Диуретический эффект не ослабевает при длительном назначении лекарства.
Гипотиазид (дихлотиазид) и циклометиазид малотоксичны и хорошо переносятся больными. Побочное влияние салуретиков выражается в гипокалиемии, развивающейся в результате усиленного выделения калия с мочой. Признаками гипокалиемии являются: слабость, сонливость, тошнота, мышечные подергивания, изменения ЭКГ (удлинение интервала P - Q, появление экстрасистолий, отрицательный зубец T). При назначении малых доз салуретиков (например, 25 мг гипотиазида) гипокалиемию можно предотвратить диетой, богатой солями калия. Они содержатся в значительных количествах в овощах: картофеле, капусте, моркови, фасоли, горохе; во фруктах, особенно в абрикосах; в крупах: пшене, овсяной; в говядине. Если назначают большие дозы гипотиазида, дефицит калия ликвидируют одновременным приемом хлорида калия по 0,5 г 4 - 6 раз в день. Оротат калия и панангин содержат меньше калия, поэтому целесообразнее использовать хлорид калия.
Гипотиазид назначают по 25 - 50 - 75 мг в сутки тощак, реже более высокие дозы - 100 - 150 - 200 мг. срез 3 - 5 - 7 дней лечения делают перерыв на 2 - 3 дня, после чего курс лечения можно повторить.
Циклометиазид в 100 раз активнее гипотиазида. Препарат назначают по одной, реже по 2 - 3 таблетки 1 раз в день. Курс лечения тот же, что и при назначении гипотиазида.
Фуросемид (лазикс) отличается от гипотиазида более выраженным диуретическим (салуретическим) эффектом, который появляется очень быстро: при приеме внутрь - в течение часа, после внутривенного введения - через несколько минут. Такая особенность действия фуросемида связана, по-видимому, с угнетением реабсорбции натрия и хлора как в проксимальных, так и в дистальных отделах извитых канальцев почек и в восходящей части петли Генле. Калийурия, появляющаяся под влиянием фуросемида, выражена не столь значительно, поскольку реабсорбция калия угнетается в меньшей степени, чем натрия. Фуросемид усиливает диурез всего на несколько часов (после внутривенного введения - не более чем на 3 ч, после перорального - не более чем на 6 ч). При ежедневном назначении препарата уже на 3-й сутки его действие ослабевает, хотя и не прекращается полностью.
Фуросемид назначают внутрь по 1 таблетке (40 мг) натощак. Если эффект недостаточен, дозу удваивают. При отеке легких назначают до 200 мг препарата. Для ускорения мочевыделения препарат вводят внутривенно али внутримышечно (1% раствор). После приема больших доз фуросемида и, следовательно, большой потери электролитов больные нередко жалуются на слабость, вялость, тошноту, олигурию, особенно если лечение не сопровождается компенсацией дефицита калия.
Мощным салуретическим диуретиком является урегит (этакриновая кислота). Урегит связывает сульфгидрильные группы в различных участках почечных канальцев, изменяет проницаемость клеточных мембран, тормозит реабсорбцию натрия в проксимальных отделах канальцев и в восходящих отделах петли Генле. Поэтому урегит (как и фуросемид) может оказывать положительное действие в тех случаях, когда гипотиазид неспособен увеличить диурез. Действие урегита начинается через 1/2 ч, достигает максимума через 2 ч и продолжается в течение 6 ч. При внутривенном введении диурез начинается и заканчивается раньше. Как и все салуретики, урегит выводит из организма значительное количество калия, поэтому его надо назначать на фоне богатой калием диеты и дополнительного введения хлорида калия.
Урегит принимают утром после еды по 0,025 - 0,05 - 0,1 г через день. Комбинация урегита с гипотиазидом способна вызвать особенно обильное мочевыделение. Одновременное назначение урегита и верошпирона не только усиливает диуретический эффект, но позволяет обойтись без дополнительного приема хлорида калия.
К мочегонным - антагонистам альдостерона относится верошпирон (альдактон, спиронолактон). Верошпирон блокирует действие альдостерона на почечные канальцы, вызывая натрийурез. Ценной особенностью верошпирона является то, что он не выводит из организма калий и не нарушает кислотно-щелочного состояния. Верошпирон - слабое мочегонное средство, выделение мочи начинает увеличиваться только на 3 - 6-й день. Поэтому его редко назначают изолированно, а сочетают обычно с другими диуретиками: гипотиазидом, фуросемидом, урегитом для усиления диуреза. Кроме того, при лечении верошпироном в сочетании с другими мочегонными или без них нет необходимости в одновременном приеме препаратов калия для профилактики гипокалиемии.
Верошпирон назначают начиная с 6 - 8 таблеток (по 25 мг каждая) в день, постепенно уменьшая дозу до 1 таблетки. Если одновременно применяют другие мочегонные, то их назначают в обычных дозах.
Бринальдикс также является препаратом, тормозящим обратное всасывание натрия и хлора, но не влияющим на экскрецию калия. Поэтому лечение бринальдиксом осуществляется без добавления препаратов калия. Под влиянием бринальдикса выраженный диуретический эффект наступает через 2 - 3 ч и длится примерно 6 - 8 ч. Препарат назначают по 1/2 - 1 таблетке (40 мг) 1 раз в день в течение 5 - 7 дней. Наибольший эффект наблюдается в первые 2 - 3 дня лечения.
Каждое из указанных средств может применяться для лечения отеков у беременных, больных гломерулонефритом. Когда нужно получить очень быстрый эффект, а также при признаках отека легких или отека мозга, предпочтительнее фуросемид, особенно парентеральное введение его. Для курсового лечения, способствующего ликвидации отеков в течение нескольких дней, используют гипотиазид, циклометиазид, гщротон, урегит, бринальдикс, верошпирон. Дозу каждого препарата для больной необходимо подбирать индивидуально, начиная со средних доз и наблюдая за терапевтическим эффектом. В отличие от ртутных диуретиков современные мочегонные средства не обладают вредным влиянием на внутриутробный плод.
Лечение гипопротеинемии заключается во вливании белковых жидкостей. Сухую плазму в разведении бидистиллированной водой в отношении 1:3 вводят по 200 - 300 мл внутривенно капельно 2 - 3 раза в неделю. С этой же целью в вену вводят 20% раствор альбумина по 100 - 200 мл или протеин по 200 - 300 мл. Небелковой природы плазмозамещающие жидкости (полиглюкин, реополиглюкин) не уменьшают белковый дефицит, и с этой целью их применять не имеет смысла.
К симптоматической терапии относится и лечение анемии при гломерулонефрите. Назначение препаратов железа (перорально, внутримышечно или внутривенно), витамина B12, фолиевой кислоты и других средств часто малоэффективно. Более надежно переливание крови или эритроцитной массы.
Как уже указывалось, патогенетическая терапия гломерулонефрита, направленная на подавление иммунологических сдвигов, во время беременности противопоказана. Кортикостероидные препараты (преднизолон, триамцинолон и др.) эффективны в больших дозах: 50 - 70 мг преднизолона в сутки на протяжении 2 нед, затем дозу уменьшают. Некоторые исследователи (Mampel, 1970; Mosler, 1970) считают допустимым назначение таких высоких доз стероидных препаратов беременным, однако подобное лечение может привести к тератогенному эффекту.
Другие иммунодепрессанты (имуран, 6-меркаптопурин), а также цитостатические средства (лейкеран, циклофосфан), препараты аминохинолинового ряда (резохин, хлорохин, делагил, плаквенил) и метиндол (индометацин) противопоказны во время беременности, так как обладают тератогенным действием.
Антибиотики не оказывают влияния на течение гломерулонефрита, как и удаление инфекционного очага (хронический тонзиллит) не излечивает нефрит. Тонзиллэктомия имеет важное профилактическое значение, если ее производят в самом начале заболевания, а при хроническом гломерулонефрите удалять миндалины во время беременности нет необходимости. При простудных, особенно стрептококковых, заболеваниях показано лечение антибиотиками, причем такими, которые оказывают наименьшее нефротоксическое действие. К ним относятся бензилпенициллин, к которому не развивается "привыкания" стрептококковой флоры, а также эритромицин. Антибиотики тетрациклинового ряда не только обладают нефротическим действием, но и неблагоприятно влияют на плод. Сульфаниламидные препараты нефротоксичны, их назначение особенно нежелательно при гломерулонефрите.
Лечение очагового нефрита предусматривает в первую очередь ликвидацию основного заболевания при помощи антибиотиков, диету с ограничением поваренной соли (до 5 г в сутки) и назначение легкоусвояемых углеводов, а также витаминов C и P. Для ликвидации гематурии аскорбиновую кислоту назначают по 0,3 г 3 раза в сутки, рутин по 0,04 г 3 раза в день и хлорид калия по 1 г 3 раза в день.
|
ПОИСК:
|
© ROGHDENIEREBENKA.RU, 2010-2019
При копировании материалов активная ссылка обязательна:
http://roghdenierebenka.ru/ 'Беременность, рождение и первые годы жизни ребёнка'
При копировании материалов активная ссылка обязательна:
http://roghdenierebenka.ru/ 'Беременность, рождение и первые годы жизни ребёнка'