
Особенности гормональных и метаболических взаимоотношений в системе мать - плод при осложненном течении сахарного диабета
Особенности гормональных и метаболических изменений у плодов, родившихся в асфиксии. Для изучения влияния, которое оказывает гипоксия на гормональные и метаболические показатели плодов, матери которых страдают сахарным диабетом, был проведен сравнительный анализ соответствующих показателей у 30 плодов, состояние которых при рождении было расценено как удовлетворительное, и у 30 плодов, родившихся с явлениями асфиксии, у 20 из них была легкая степень асфиксии и у 10 - тяжелая. Полученные результаты представлены в табл. 8.

Таблица 8. Содержание гормонов в крови матерей, больных сахарным диабетом, и их новорожденных в зависимости от состояния ребенка при рождении
Из данных табл. 8 следует, что для плодов, родившихся с явлениями легкой асфиксии (оценка по шкале Ангар 5 - 6 баллов), было характерно несколько более высокое содержание ПРИ (114% при асфиксии и 100% при удовлетворительном состоянии новорожденного), которое тем не менее не отражало истинной секреторной активности β-клеток поджелудочной железы плода, так как уровень С-пептида в этой группе был снижен (63%).
Вопрос о влиянии гипоксии на островковый аппарат поджелудочной железы плода до настоящего времени изучен недостаточно. В эксперименте [Baum et al., 1980] установлено, что наличие острой гипоксии плода приводит к незначительному повышению уровня инсулина, а при хронической гипоксии базальный уровень инсулина не меняется, хотя подавляется его реакция на гипергликемию. В противоположность этому А. К. Устинович и соавт. (1981) сообщили о снижении уровня инсулина при легкой асфиксии новорожденных, которое они связывали с гипоксическим влиянием на островковый аппарат. Согласно нашим данным, ослабление анаболического действия инсулина в этой ситуации можно рассматривать как проявление механизма адаптации, направленного на мобилизацию энергетических ресурсов организма, потребность в которой возникает в связи с энергетически неэкономным усилением процессов анаэробного гликолиза.
В то же время секреторная активность гормонов гипофизарно-надпочечниковой системы у плодов этой группы характеризовалась незначительным повышением уровня СТГ (до 110%) и кортизола (до 106,5%), а также несколько более выраженным увеличением относительной активности адренергического звена САС (коэффициент А/НА при наличии легкой асфиксии составлял 2,93, а у плодов, родившихся в удовлетворительном состоянии, он был равен 1,59).
Благодаря своей высокой лабильности САС является основной адаптационной системой, обеспечивающей постоянство внутренней среды организма в условиях стресса. Острое нарушение циркуляции крови в сосудах пуповины и маточно-плацентарного круга кровообращения, обусловленное гипоксией, сопровождается рефлекторной стимуляцией баро- и хеморецепторов, что вызывает активацию САС с повышением секреции КА. Этот процесс носит компенсаторный характер и направлен на улучшение кровоснабжения жизненно важных органов плода.
В этих условиях наиболее значительную роль играет "гормон стресса" - адреналин, поэтому при асфиксии плода преобладание относительной активности гормонального или медиаторного звена САС имеет важное значение. О значительном повышении уровня КА в пуповинной крови плодов, рожденных в состоянии легкой асфиксии от здоровых матерей, сообщали многие исследователи [Грищенко В. И. и др., 1970; Быкова Г. Ф., 1973; Lagerkrantz et al., 1980, и др.]. На основании полученных нами данных степень компенсаторного повышения уровня КА, так же как и других гормонов гипофизарно-надпочечниковой системы, у плодов, матери которых страдают сахарным диабетом, при легкой гипоксии относительно невелика. По нашему мнению, это можно рассматривать как проявление недостаточности адаптационных механизмов у этих детей.
Как и можно было предположить, гормональные изменения у перенесших асфиксию плодов от больных сахарным диабетом матерей сопровождались различными метаболическими нарушениями. Так, уровень глюкозы в пуповинной крови новорожденных, перенесших легкую асфиксию, в момент рождения составлял 2,2±0,25 ммоль/л, через 6 - 12 ч - 2,75±0,18 ммоль/л, на 3-и сутки 3,13±0,24 ммоль/л. При отсутствии асфиксии эти показатели -были равны 4,4±0,24, 2,36±0,14 и 3,24±0,16 ммоль/л.
При исследовании электролитного баланса нами было установлено, что у плодов, родившихся в состоянии асфиксии, которая сопровождалась умеренным метаболическим ацидозом (BE 12 - 18 мкв/л), уровень калия в плазме крови достигал 6,67±0,81 ммоль/л, а в эритроцитах 88,43±1,12 ммоль/л, в то время как при отсутствии асфиксии соответствующие показатели были равны 5,63±0,34 и 90,5±6,5 ммоль/л. Отношение калий эритроцитов/калий плазмы составляло соответственно 13,3 и 16, что свидетельствовало о повышении выхода калия из клеток.
Метаболизм натрия у тех же новорожденных характеризовался несколько более повышенным переходом натрия в эритроциты (21,3±2,16 и 16,3±3,7 ммоль/л) и небольшой гипернатриемией, что способствовало нарастанию внутри- и внеклеточного отека и ухудшению процессов микроциркуляции. У новорожденных, родившихся в легкой асфиксии, отмечено увеличение содержания всех липидных фракций крови.
Как видно из результатов проведенного нами анализа, преобладание у плодов, родившихся в состоянии легкой асфиксии, процессов липолиза может быть обусловлено снижением секреторной активности инсулярного аппарата и повышением воздействия контринсулярных липолитических гормонов.
Таким образом, полученные данные свидетельствуют о том, что при легкой степени асфиксии у плодов как больных, так и здоровых матерей происходит активация эндокринной системы, которая путем воздействия на определенные ферментативные системы способствует наиболее экономичной перестройке процессов метаболизма, направленных на поддержание гомеостаза в условиях кислородной недостаточности. Однако при одинаковой направленности этих реакций степень их выраженности у новорожденных обеих групп была неравнозначна, что снижает компенсаторную направленность и обусловливает более тяжелое течение неонатального периода у потомства больных сахарным диабетом матерей.
При тяжелой асфиксии плода (оценка по шкале Апгар менее 5 баллов) были выявлены значительное уменьшение содержания ПРИ (45,5%) и снижение уровня АКТГ (73%), содержание же кортизола у плодов с тяжелой асфиксией и родившихся в удовлетворительном состоянии было практически одинаковым.
Функциональное состояние САС характеризовалось глубоким угнетением ее адреналового звена: содержание А составляло 33% по сравнению со 100% у плодов, родившихся без асфиксии, а коэффициент А/НА, позволяющий судить об относительной активности звеньев САС, составил при тяжелой асфиксии плодов от больных сахарным диабетом матерей 0,68, в то время как у плодов, рожденных в удовлетворительном состоянии, он был равен 1,59, а при легкой асфиксии - 2,59.
У детей основной группы, перенесших тяжелую асфиксию, уровень гликемии как при рождении, так и в течение первой недели! жизни был низким. Наряду с этим отмечено значительное уменьшение содержания всех липидных фракций, особенно СЖК (0,18±0,04 г/л). Убедительным свидетельством снижения при гипоксии интенсивности компенсаторных процессов липолиза является также выявленное нами у плодов основной группы достоверное снижение уровня цАМФ (15,4±3,68 нг/мл при тяжелой асфиксии и 27,22±0,96 нг/мл при удовлетворительном состоянии плода). Липолитический эффект таких гормонов, как адреналин, глюкагон, АКТГ, обусловлен активностью цАМФ.
Аналогичные данные были получены нами при исследовании белкового и электролитного метаболизма. Так, содержание белка в пуповинной крови плодов составило 51,3±10,2 г/л, а уровень калия в плазме снизился до 5,47±1,2 ммоль/л.
Таким образом, при сахарном диабете матери состояние гормонального и метаболического статуса плодов, родившихся в тяжелой асфиксии, свидетельствует о его глубоком угнетении и наступившем срыве их адаптационных механизмов.
Можно полагать, что при сахарном диабете наиболее частыми причинами развития гипоксии плода являются не акушерские осложнения, а появление у рожениц нераспознанных еще клинически метаболических изменений (например, гипогликемическое состояние), которые сопровождаются соответствующими компенсаторными реакциями со стороны гормонов контринсулярной системы матери и плода.
Полученные данные позволяют проследить связь между гормональными и метаболическими изменениями у больных сахарным диабетом матерей и состоянием новорожденного. В связи с этим компенсация сахарного диабета у матери во время беременности и в родах является одновременно профилактикой возникающих в родах осложнений со стороны матери и плода.
Особенности гормональных и метаболических изменений у матери и плода при сахарном диабете, осложненном микроангиопатиями. В центре внимания современной диабетологии находится проблема сосудистых осложнений диабета, определяющих не только трудоспособность больных, прогноз заболевания, но и продолжительность их жизни.
Частота сосудистых осложнений у больных сахарным диабетом может достигать 90 - 97%, при этом частота диабетического гломерулосклероза колеблется от 22 до 63%. Наиболее часто встречающимся сосудистым осложнением диабета является поражение мелких сосудов (микроангиопатии). Патология мелких артериол и капилляров с утолщением базальной мембраны, пролиферацией эндотелия и накоплением ШИК-положительного вещества характерна для диабета с распространенным процессом. Чаще всего встречаются различные варианты изменений мелких сосудов сетчатки глаза (диабетическая ретинопатия) и почечных клубочков (диабетическая нефропатия). Нередко наблюдается и микроангиопатия нижних конечностей.
Достаточно часто выявляются диабетические микроангиопатии и у беременных, страдающих сахарным диабетом. По данным С. В. Уголевой и соавт. (1982), в группе беременных, заболевших сахарным диабетом до 15-летнего возраста, диабетическая ретинопатия встретилась у 47%, а диабетическая нефропатия - у 13% больных. Cassar и соавт. (1978) наблюдали проявления диабетической микроангиопатии примерно у 25% больных с детским и юношеским диабетом. Согласно данным В. Н. Зубкова (1980), у всех беременных, больных сахарным диабетом с детского и юношеского возраста, наблюдались те или иные проявления сосудистой патологии, при этом наиболее тяжелые формы диабетической микроангиопатии (пролиферирующая ретинопатия и диабетическая нефропатия) были отмечены у 13 из 85 беременных. По мнению большинства авторов, влияние сосудистых осложнений диабета на течение беременности проявляется высокой частотой тяжелых форм сочетанных токсикозов и с трудом поддающихся лечению пиелонефритов. Для того чтобы выяснить, какое влияние оказывает наличие сосудистых осложнений диабета на функциональное состояние эндокринной системы матери и плода, был проведен сравнительный анализ гормонального статуса 15 рожениц с тяжелой формой сахарного диабета, заболевание у которых осложнилось диабетической ретино- и нефропатией (I группа) и 26 рожениц с тяжелой формой неосложненного сахарного диабета (II группа). Аналогичному исследованию подверглись и плоды этих женщин. Полученные данные представлены в табл. 9.
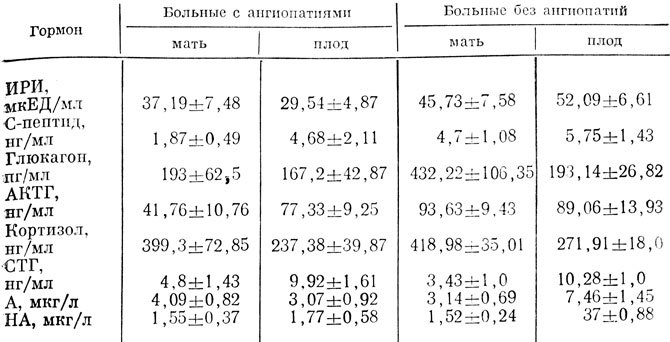
Таблица 9. Особенности гормональных изменений у рожениц, больных сахарным диабетом, и их плодов в зависимости от наличия сосудистых осложнений
Из данных табл. 9 видно, что у рожениц I группы наблюдалась явная тенденция к снижению секреторной активности исследуемых эндокринных систем (исключение составили симпатико-адреналовая система и продукция гипофизом соматотропного гормона). Так, при наличии диабетической микроангиопатии содержание гормонов, секретируемых α- и β-клетками поджелудочной железы, составляло соответственно 45 и 82% по отношению к принятому за 100% уровню глюкагона и ПРИ у рожениц с неосложненным диабетом, при этом уровень C-пептида у больных I группы был в 21/2 раза ниже, чем во II. Следовательно, у рожениц с диабетическими ретинопатиями и нефропатиями секреторные резервы инсулярного аппарата и остаточная секреция инсулина оказались значительно сниженными.
Уровень гормонов гипофиза и надпочечников у рожениц I группы по отношению к принятым за 100% соответствующим показателям у больных неосложненным диабетом составлял: СТГ 140%, АКТГ 45%, кортизола 95%. На фоне умеренного повышения уровня А (130%) и практически одинакового содержания НА (102%) у рожениц с диабетическими микроангиопатиями отмечается более выраженное отношение А/НА (2,26 и 2,06), что свидетельствует о преобладании адренергических влияний и напряжении конечных этапов биосинтеза КА.
Таким образом, у рожениц с тяжелой формой сахарного диабета, осложненного диабетическими микроангиопатиями, на фоне общего снижения гормональной активности β-клеток поджелудочной железы (абсолютная инсулиновая недостаточность) отмечается тенденция к снижению активности контринсулярной гипофизарно-надпочечниковой системы. В то же время в ответ на аварийную ситуацию (инсулиновая недостаточность) активируется наиболее лабильная адаптационная симпатико-адреналовая система и повышается относительная активность ее адренергического звена. На фоне сниженной общей гормональной активности обращает на себя внимание некоторое повышение концентрации СТГ, который принимает участие в патогенезе сосудистых осложнений при диабете. Таким образом, полученные данные свидетельствуют о снижении резервных возможностей гипофизарно-надпочечниковой системы, прогрессирующей по мере увеличения тяжести диабета и присоединения сосудистых осложнений.
По мнению А. С. Ефимова (1982), в комплексе факторов, приводящих к развитию диабетических микроангиопатий, помимо генетических дефектов сосудистой стенки и присущих декомпенсации диабета обменных нарушений, существенную роль играет избыток не только СТГ, но и кортизола. Не исключена также роль активации адренергического звена САС. Можно предположить, что выявленная нами у обследованных беременных и рожениц на фоне нарастающей инсулиновой недостаточности и умеренного повышения соматотропной и адренергической активности тенденция к снижению синтеза гормонов гипофизарно-надпочечниковой системы обусловлена присоединением таких стрессовых факторов, как беременность и роды.
Как показали наши исследования, у беременных и рожениц с сахарным диабетом, осложненным диабетическими микроангиопатиями, нередко возникают также изменения липидного спектра крови, которые проявляются нерезко выраженным увеличением всех липидных фракций, особенно СЖК. Так, показатели липидограммы крови у беременных с диабетическими микроангиопатиями составляли: фосфолипидов 281,4±14,7 мг%, свободного холестерина 118,0+16,4 мг%, СЖК 95,4± 16,9 мг%, ТГ 251,4+28,8 мг%, эфиров холестерина 272,1±36,7 мг%, общих липидов 1018,2±26,2 мг%. Соответствующие показатели у беременных с тяжелой формой сахарного диабета без ангиопатии равнялись 266,0±18,9; 90,5±5,2; 54,2±5,0; 230,7±18,8; 270,1±16,5 и 911,5±24,6 мг%. Более выраженное увеличение СЖК у беременных с диабетическими сосудистыми осложнениями по сравнению с больными неосложненным диабетом свидетельствует о преобладании у первых липолитических процессов что обусловлено, вероятно, более выраженной инсулиновой недостаточностью.
В свою очередь активация липолиза способствует повышению в крови уровня холестерина, который является одним из факторов, участвующих в развитии диабетической ангиопатии. Таким образом, необходимой мерой профилактики сосудистых осложнений у больных сахарным диабетом беременных следует считать максимальную компенсацию липидного обмена.
Влияние сосудистых осложнений матерен, больных сахарным диабетом, на гормональный статус их детей нашло свое отражение в снижении секреторной активности их поджелудочной железы: ИРИ до 76%, С-пептида до 81%), глюкагона до 87%.
Снижение секреторной активности инсулярного аппарата, гипофизарно-надпочечниковой, а также симпатико-адреналовой систем у плодов от матерей с осложненным сахарным диабетом свидетельствует о некотором снижении гормонального влияния матери на плод (менее выражены гипериисулинизм и гиперкортицизм). Это проявляется клинически в снижении массы тела плодов: средняя масса тела плодов при диабетической ангиопатии матери составляет 3020±80 г, в то время как масса плодов от матерей без сосудистых осложнений того же гестационного возраста равна 3650±109 г. В то же время снижение активности симпатико-адреналовой и гипофизарно-надпочечниковой систем приводит к нарушениям адаптационных процессов в постнатальном периоде у новорожденных, родившихся от матерей с диабетическими осложнениями.
Выявленные изменения гормонального статуса плодов от матерей, больных сахарным диабетом, осложненным диабетической микроангиопатией, вызывают нарушения метаболизма у этих детей. Особенно ярко это проявляется при сравнительном анализе липидного обмена, почти все показатели которого по сравнению с таковыми у плодов от матерей с неосложненным диабетом оказались сниженными. Например, содержание фосфолипидов в крови у плодов I группы составляло 118,6± 12,3 мг%, свободного холестерина- 58,4±2,6 мг%, СЖК - 21,8 16 мг%, ТГ - 49,4±2,6 мг%, эфиров холестерина - 138,1±12,8 мг%, общих липидов 385,2±8,2 мг%. Соответствующие показатели у плодов II группы равнялись соответственно 148,9±6,3; 62,8±7,2; 26,3±1,8; 58,1±1,3; 149,1±15,2 и 445,2±9,8 мг%.
При мониторном наблюдении за плодами от матерей с сосудистыми осложнениями выявлено преобладание силентного типа осцилляций - 52±12% (очень узкая лента записи КТГ), ухудшение двигательной активности (4 - 6 шевелений за время записи), отсутствие компенсаторных реакций на шевеление. Соответствующие показатели КТГ у плодов от матерей с неосложненным сахарным диабетом были следующими: плотность силентного типа осцилляций 23,4±6%, 8 - 12 шевелений, наличие компенсаторных реакций в ответ на шевеление. Результаты мониторного наблюдения свидетельствуют о выраженной хронической гипоксии у плодов от матерей с сосудистыми осложнениями диабета.
Таким образом, у плодов от матерей с диабетическими ангиопатиями на первый план выступают не нарушения метаболизма, а явления хронической гипоксии, что, по-видимому, объясняется склеротическими изменениями сосудов плаценты. В связи с этим для улучшения функционального состояния плодов от матерей с сосудистыми осложнениями диабета в первую очередь необходима компенсация липидного и связанного с ним углеводного обмена матери, а также применение сосудорасширяющих средств, нормализующих маточно-плацентарное кровообращение.
Особенности гормональных и метаболических изменений у больных сахарным диабетом матерей и их плодов при декомпенсации диабета. Для изучения влияния, которое оказывает на состояние эндокринной системы и обменные процессы плода степень компенсации диабета у матери, мы провели сравнительный анализ гормональных и метаболических изменений у плодов от рожениц с хорошо компенсированным (уровень гликемии 5,5±0,11 ммоль/л) заболеванием (I группа) и декомпенсированным (уровень гликемии 11,0±0,11 ммоль/л) во время беременности диабетом (II группа).
В результате проведенных исследований было установлено, что при высокой гликемии матери во время беременности у плодов отмечаются резкое повышение секреторной активности инсулярного аппарата, небольшое увеличение уровня контринсулярных гормонов гипофиза и надпочечников, а также заметный подъем концентрации адреналина в крови. Так, по сравнению с принятым за 100% уровнем гормонов в пуповинной крови плодов I группы соответствующие показатели у плодов II группы составили: ИРИ 438%, С-пептида 480%г СТГ 139,7%, АКТГ 122% и кортизола 129%. При этом концентрация А и НА достигала во II группе соответственно 171 и 111%, а величина коэффициента А/НА, характеризующего степень относительной активности отдельных звеньев САС, была равна 3,27 (у плодов I группы 2,15) (табл. 10).
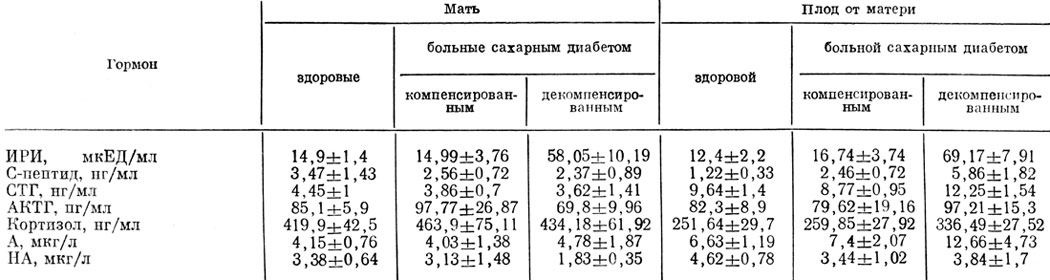
Таблица 10. Содержание гормонов в крови матери и плода при компенсированном и декомпенсированном диабете
Выявленное у плодов от матерей с высокой гипергликемией, отмечавшейся во время беременности, преобладание адренергического влияния или наличие гормонально-медиаторной диссоциации (увеличение содержания А, которое не сопровождается соответствующим повышением уровня НА) следует рассматривать как защитную реакцию на выраженный метаболический стресс, при которой ведущая роль принадлежит адреналину. Таким образом, при декомпенсированном во время беременности сахарном диабете матери отмечается высокое напряжение функциональной активности гормональных систем плода.
В то же время отношения уровней ИРИ и С-пептида к сумме концентраций контринсулярных гормонов, позволяющие косвенно судить о преобладающей секреторной активности инсулярной или контринсулярной систем, у плодов I и II групп были соответственно равны: ИРИ/СТГ+АКТГ+К+А 0,007 и 0,013; С-пептид/СТГ+АКТГ+К+А 0,047 и 0,15; C-пептид/гликемия 0,61 и 0,99.
Полученные данные свидетельствуют о наличии при декомпенсированном диабете матери значительного напряжения секреторной активности инсулярного аппарата плода. Состояние метаболизма плодов II группы характеризовалось высоким уровнем гликемии (содержание глюкозы в пуповинной крови плодов I и II групп соответственно 4,0±0,25 и 5,9±1,2 ммоль/л, P<0,05) и нерезко выраженным увеличением содержания всех липидов. Следовательно, если при неосложненном сахарном диабете матери наблюдается преобладание у плодов липосинтетических процессов, то при декомпенсации диабета у плодов отмечено преобладание процессов липолиза. Увеличение активности катаболических процессов у плодов II группы было подтверждено нами и при изучении аминокислотного и белкового состава крови. Так, при компенсированном и декомпенсированном сахарном диабете матери суммарная концентрация свободных аминокислот в пуповинной крови плодов составляла соответственно 100 и 110%, что свидетельствует о менее активной их утилизации последними. При этом уровень протеинемии во II группе был достоверно ниже (80%), чем в I (100%).
Как показали результаты наших исследований, электролитный состав крови у плодов от матерей с декомпенсированным во время беременности диабетом характеризовался небольшим снижением концентрации ионов калия (К+) в клетках. Так, содержание К+ в эритроцитах у плодов I и II групп составило соответственно 93±2,9 и 89,2±3,3 ммоль/л. У последних выявлено статистически значимое повышение плазменной концентрации K+ (соответственно 5,6±0,3 и 7,6±0,6 ммоль/л). В результате повышенного выхода из клеток K+ активизируются процессы диффузии из внеклеточной жидкости в клетки ионов натрия (Na+) (17,8±1,4 ммоль/л ори компенсированном и 19,2±0,5 ммоль/л при декомпенсированном диабете матери). Это повлекло за собой снижение содержания Na+ в плазме крови (соответственно 139,6±1,9 и 130,6±3,5 ммоль/л).
Убедительным подтверждением выявленной закономерности может служить сравнение в обеих группах трансмембранных градиентов по K+ и Na+, характеризующих распределение ионов по обе стороны клеточной мембраны. Так, коэффициент К+ эритроцитов/К+ плазмы, составлявший в I группе 16,8, при декомпенсированном диабете матери был снижен до 12,6. Соответствующие коэффициенты Na+ плазмы крови/Na+ эритроцитов были равны 7,84 и 6,8.
Таким образом, полученные данные позволяют сделать вывод о наличии у плодов при декомпенсации диабета матери относительного клеточного дефицита K+ в сочетании с истинной гиперкалиемией и статистически достоверной гипонатриемией. В связи с высокой гидрофильностью Na+ избыточное поступление их в клетки обусловливает нарастание внутриклеточного отека, что способствует нарушению микроциркуляции и развитию циркуляторной гипоксии. Кроме того, весьма тяжелым последствием выявленных на уровне клеточной мембраны ионных перераспределений являются возможные сдвиги в трансмембранном переносе глюкозы. Известно, что транспорт K+ в клетки связан с переходом в них глюкозы.
Значительную роль в переносе глюкозы играют также ионы Na+, вовлекающие вслед за собой в клетку глюкозу. При выходе из клетки Na+ способствует выведению из клеток продуктов клеточного метаболизма. Развившаяся у плодов при декомпенсации диабета матери гиперкалиемия затрудняет эти процессы, что, несмотря на высокий уровень глюкозы в плазме крови, способствует развитию клеточного дефицита глюкозы.
Характерные для плодов от матерей с декомпенсированным во время беременности диабетом метаболические нарушения (гипергликемия и гиперкалиемия) позволяют объяснить и выявленные нами сдвиги одной из самых филогенетически древних и самых жестких констант организма - осмолярности крови. Так, согласно полученным в нашей клинике данным (Н. П. Кирбасова), осмолярность пуповинной крови, которая у плодов от здоровых матерей составила 298,4±6,2 мосм/л, у плодов от матерей с компенсированным сахарным диабетом была равна 307,97±2,76 мосм/л, а при декомпенсированном диабете достигала 314,19±4,1 мосм/л. Выявленное статистически значимое повышение осмолярности крови у плодов свидетельствует о наличии развившихся внутриутробно очень тяжелых обменных нарушений, поэтому это явление можно рассматривать как прогностически крайне неблагоприятный признак.
Следовательно, на фоне выявленного нами у плодов от матерей с декомпенсированным течением диабета резкого повышения секреторной активности инсулярного аппарата, которое сопровождалось более умеренным увеличением уровня контринсулярных гормонов, отмечалось увеличение содержания глюкозы в пуповинной крови, усиление процессов липолиза и катаболизма белка, снижение утилизации аминокислот, нарушение ионного перераспределения на уровне клеточной мембраны, а также значительное повышение осмолярности плазмы крови (рис. 3). Для состояния обменных процессов матерей было характерно достоверное повышение уровня гликемии: при компенсированном диабете 4,8±0,37 ммоль/л, при декомпенсированном 9,2±0,7 ммоль/л (P<0,001).
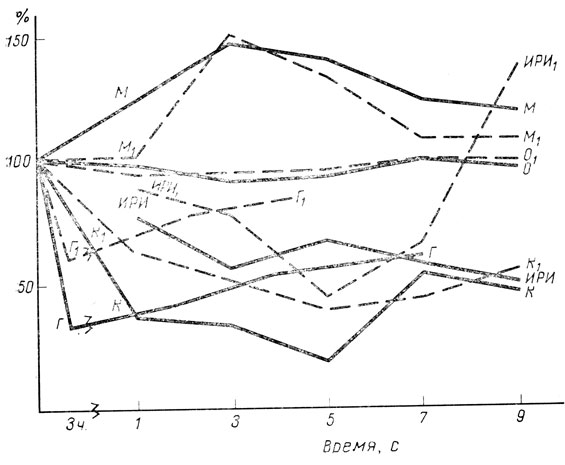
Рис. 3. Особенности гормональных и метаболических изменений новорожденных от матерей с компенсированным и декомпенсированным во время беременности диабетом. Пунктирные кривые - новорожденные от матерей с компенсированным сахарным диабетом; сплошные кривые - новорожденные от матерей с декомпенсированным диабетом. ПРИ, ИРИ1 - иммунореактивный инсулин, K, K1 - кортизол, Г, Г1 - гликемия, О, О1 - осмолярность, M, M1 - мочевина
В то же время небольшое увеличение суммарного содержания в крови свободных аминокислот (132% по отношению к принятому за 100% уровню при компенсированном диабете), статистически значимое повышение уровня мочевины (9,86±0,7 и 6,8±0,64 ммоль/л) и наличие достоверно более выраженной гипопро- теинемии (75,6±2,1 и 84,9±3,6 г%) свидетельствуют о сниженной утилизации аминокислот и нарушении синтеза белка.
Наряду с этим в крови больных матерей были отмечены вызванные инсулиновой недостаточностью изменения ионных соотношений. Так, при декомпенсированном диабете уровень K+ в плазме крови был достоверно повышен (158%), а в эритроцитах снижен (81,6%) по сравнению с таковыми при компенсированном течении заболевания (100%).
В соответствии с принципом конкурентности ионов у рожениц с декомпенсированным во время беременности заболеванием отмечено накопление в клетках Na+ (152%, P<0,002) и уменьшение их в плазме (87%, P<0,01). У них повышается также осмолярность плазмы (3284=7,2 и 307,844=6,65 мос/л; P<0,05).
Повышение уровня гликемии, активизация процессов липолиза, нарушение белкового синтеза, наличие выраженной трансминерализации - все эти метаболические нарушения у рожениц с декомпенсированным сахарным диабетом являются результатом значительного снижения анаболического эффекта инсулина вследствие тяжелой инсулиновой недостаточности.
Убедительным свидетельством наличия у рожениц этой группы выраженного истощения инсулярного аппарата явилось снижение у них секреции C-пептида (2,37±0,89 нг/мл при декомпенсированном, 2,56±0,72 нг/мл при компенсированном диабете и 3,47±1,4 нг/мл в контроле).
Таким образом, проведенные нами исследования позволили выявить наличие у матери с декомпенсированным диабетом и плода одинаковой направленности метаболических изменений - повышенной активности катаболических процессов.
Выявленные у плодов от матерей с декомпенсированным во время беременности диабетом усиление процессов липолиза, катаболизма белка и сдвиги электролитного баланса в сторону повышенного выхода калия из клеток могут быть обусловлены либо недостаточным анаболическим действием инсулина, либо резким усилением липолитического влияния контринсулярных гормонов, в частности глюкокортикоидов. Судя по величине коэффициента С-пептид/СТГ+АКТГ+К+А, который был равен 0,047 в I и 0,15 во II группе, отношение секреции (3-клеток к величине секреторной активности всех контринсулярных гормонов у плодов II группы был почти в 3 раза выше, чем при компенсированном диабете матери, что противоречит предположению о чрезмерном усилении липолитического влияния контринсулярных гормонов плода.
Это позволяет считать, что в основе выявленной у плодов от матерей с декомпенсированным во время беременности диабетом активизации процессов катаболизма лежит уменьшение анаболического действия инсулина. Снижение биологической активности фетального инсулина на фоне выраженной гиперфункции инсулярного аппарата плода, по-видимому, может явиться или результатом переключения его действия, направленного на снижение гипергликемии матери, или возможного понижения чувствительности рецепторов клеточных мембран к инсулину (относительная инсулиновая недостаточность). Таким образом, декомпенсацию диабета матери следует расценивать как угрозу развития относительной инсулиновой недостаточности плода.
У плодов от матерей с компенсированным во время беременности сахарным диабетом многие гормональные и метаболические показатели приближались к данным, характерным для плодов от здоровых матерей. Так, содержание ИРИ с С-пептида в пуповинной крови плодов при компенсированном диабете матери составляло соответственно 134,8 и 201% (при 100% в контроле), а уровень гормонов гипофизарно-надпочечниковой системы практически не отличался от такового в контроле, за исключением содержания СТГ, которое было несколько уменьшено (90,9%).
Функциональное состояние САС обследованных плодов также характеризовалось незначительным изменением содержания в крови КА (А 111,6%, НА 91,9%). Коэффициент А/НА, характеризующий относительную активность звеньев САС, был равен 1,43 (в контроле 1,43). Содержание глюкозы в пуповинной крови плодов составило 4,0±0,25 ммоль/л (у плодов здоровых матерей 4,3±0,39 ммоль/л).
Белковый состав крови плодов от матерей с компенсированным во время беременности течением диабета также приближался к таковому у плодов контрольной группы. Так, уровень общего белка в пуповинной крови плодов I группы составлял 66,7±3,7 г/л, что было приблизительно равно показателю у плодов здоровых матерей. Концентрация альбумина при компенсированном диабете матери равнялась 63,76±1,43% (в контроле 60,1±1,11%) и глобулина - соответственно 36,24±1,43 и 39,9±1,11%. Следовательно, эти изменения были незначительными. Обращало на себя внимание то обстоятельство, что содержание фетального у-глобулина (13,19±0,61%) практически не зависело от степени компенсации диабета у матери, но было заметно меньше (79%), чем в контроле. Очевидно, снижение уровня у-глобулина крови отражает тормозящее влияние заболевания матери на иммунные процессы плода.
Более выраженные изменения были отмечены со стороны липидного и электролитного состава крови. Так, уровень СЖК и ТГ в пуповинной крови плодов от матерей с компенсированным во время беременности сахарным диабетом составлял соответственно 0,27±0,03 г/л и 0,7±0,1 ммоль/л (в контроле 0,2±0,01 г/л и 0,46±0,03 ммоль/л).
В то же время при сравнении данных ионограмм плодов от здоровых и больных компенсированным сахарным диабетом матерей у последних было отмечено более высокое содержание K+ в плазме крови (5,6±0,26 и 4,8±0,15 ммоль/л), а также снижение мембранного градиента как по K+ (соответственно 16,7 и 18,7), так и по Na+ (7,8 и 11,7). Эти изменения свидетельствуют о неполной нормализации ионных соотношений у обследованных женщин.
Таким образом, у плодов от матерей с декомпенсированным во время беременности диабетом под влиянием длительных метаболических нарушений развивается повышенная секреторная активность инсулярного аппарата, индуцированная поступлением от матери больших количеств глюкозы. При этом, несмотря на общеизвестный анаболический эффект инсулина, у этих плодов на фоне гиперинсулинизма отмечается повышение уровня гликемии, усиление процессов липолиза, ухудшение утилизации аминокислот, нарастание гемопротеинемии и появление трансминерализации" Эти нарушения свидетельствуют о выраженных катаболических нарушениях обменных процессов, аналогичных таковым у их матерей, что приводит к развитию у части этих детей гиперосмолярного состояния.
Полученные данные позволяют высказать предположение о снижении у плодов при декомпенсации диабета матери биологического эффекта инсулина, т. е. о развитии у них относительной инсулиновой недостаточности.
Это приводит к затруднению становления процессов адаптации, нарушению гомеостаза (развитие гиперосмолярного синдрома), а в особо тяжелых случаях - к истощению секреторной активности β-клеток поджелудочной железы. Кроме того, в раннем неонатальном периоде в связи с прекращением трансплацентарного перехода глюкозы от матери к плоду развившийся еще внутриутробно гиперинсулинизм может привести к возникновению тяжелых гипогликемических состояний новорожденного. Следовательно, при декомпенсации диабета матери ребенок находится под неблагоприятным воздействием двух факторов: относительной инсулиновой недостаточности (до рождения) и выраженного следового гиперинсулинизма в первые дни неонатального периода.
На основании полученных результатов можно считать, что основной мерой профилактики перинатальной заболеваемости и смертности детей при сахарном диабете матери является обязательная компенсация заболевания матери, при которой должна быть достигнута нормализация показателей не только углеводного, но и других видов обмена веществ.
|
ПОИСК:
|
© ROGHDENIEREBENKA.RU, 2010-2019
При копировании материалов активная ссылка обязательна:
http://roghdenierebenka.ru/ 'Беременность, рождение и первые годы жизни ребёнка'
При копировании материалов активная ссылка обязательна:
http://roghdenierebenka.ru/ 'Беременность, рождение и первые годы жизни ребёнка'