
Глава I. Анатомия миометрия и нейрогуморальная регуляция сократительной функции матки
Строение миометрия
Матка обладает способностью сокращаться в течение всего детородного периода жизни женщины, на протяжении менструального цикла, в период беременности, родов и в послеродовом периоде. Наибольшей выраженности эта способность достигает в родах. В послеродовом периоде активность матки постепенно снижается, возвращаясь к уровню, характерному для небеременной матки.
На сократительную способность миометрия большое влияние оказывают гормональные, нейрогенные и гуморальные факторы. Поскольку миометрий участвует в нейроэндокринном половом цикле и осуществлении репродуктивной функции, его изменения (как органа, удерживающего и изгоняющего плодное яйцо) очень важны в сохранении специфических функций женского организма.
Матка представляет собой полый орган, образованный из гладкомышечной, соединительной (коллагеновой) и эластической ткани. Длина матки вне беременности 7 - 8 см, ширина 5 - 6 см, переднезадний размер 3 - 4 см; 2/3 длины матки приходятся на тело, 1/3 - на перешеек и шейку. При гипоплазии матки наблюдается обратное соотношение длины тела и шейки.
В матке различают: дно, тело, перешеек и шейку (надвлагалищная и влагалищная части). Во время беременности из нижней части тела, перешейка и надвлагалищной части шейки матки формируется так называемый нижний сегмент матки, который вместе с телом матки составляет плодовместилище.
Различают также переднюю и заднюю поверхности матки, правое и левое ребро, трубные углы, откуда отходят придатки матки - маточная труба, собственная связка яичника и яичник. На шейке имеется передняя и задняя губы, между которыми находится шеечный канал, соединяющий полость матки с влагалищем. Наружный зев шейки матки у нерожавших женщин имеет поперечно-овальную форму, а у рожавших - щелевидную вследствие надрывов, произошедших в родах.
Перешеек матки является частью шейки матки. Верхняя граница перешейка с телом матки называется внутренним анатомическим зевом, место перехода слизистой оболочки матки в слизистую канала шейки матки гистологическим зевом. Их границы не совпадают. Передняя стенка шейки матки тоньше, чем задняя, и легче растягивается в родах. Перешеек открывается кверху в полость матки через анатомический внутренний зев, книзу в канал шейки матки через гистологический зев.
Снаружи тело матки покрыто серозным покровом брюшины, передний и задний листки которой у боковых поверхностей матки соединяются, образуя широкие связки. Листки широких связок переходят на стенки малого таза. Между листками широких связок проходят сосуды и нервы.
Толщина мышечного слоя в дне матки 1,5 - 2 см у небеременной и 4 - 5 см у беременной женщины. В средней части тела матки на протяжении всей ее длины миометрий более компактный, с боков (ребра тела матки, нижнего сегмента и шейки) - менее компактный вследствие вхождения в толщу его сосудов (здесь он легче рвется).
Миометрий имеет сложное строение: волокна гладкомышечных пучков расположены в разных направлениях. Сложность анатомической структуры матки обусловлена тем, что ее верхний (дно, тело), и нижний (перешеек, шейка) сегменты выполняют разные функции: верхний сегмент - изгоняющую или сохраняющую, нижний соответственно - "открывательную" либо "запирательную") Фетальная матка в антенатальном периоде развивается из двух парамезонефрических (мюллеровых) протоков. На 8-й неделе гестационного периода образуются шейка и перешеек матки, тело ее рудиментарно; позже во 11 триместре беременности (26 - 28 нед), формируются дно и тело матки (архимиометрий), при этом слои миометрия прорастают друг в друга и между ними нет резкой границы. Степень слияния парамезонефрических протоков у млекопитающих различна. Вследствие неполного слияния протоков у человека могут возникнуть пороки развития или врожденная неполноценность структуры и формы матки (седловидная, двурогая, гипопластичная). Влияние повреждающих факторов на плод в период роста тела матки и наружной зоны миометрия (гестационный возраст плода 26 - 28 нед) может обусловить врожденную несостоятельность матки. В будущем у такой женщины отмечается нарушение функции матки (невынашивание и недонашивание беременности, инертность матки в родах, дискоординированная родовая деятельность).
В связи с этим при сборе анамнеза следует обращать особое внимание на массу тела пациентки при рождении, здоровье ее матери, характер нарушений течения беременности и родов, при которых родилась пациентка, особенности развития и перенесенные заболевания в подростковом и юношеском возрасте, начало становления менархе и характер менструального цикла. Необходимо учитывать, что постпонирующий (29 - 35 дней) и антипонирующий (21 - 27 дней) менструальные циклы нельзя в полной мере считать нормальными. Часто они являются свидетельством того, что регуляция деятельности половой системы женщины со стороны нейроэндокринной системы неустойчива. Важно также установить, через какой срок от начала половой жизни наступила первая беременность и чем она окончилась, как протекали предыдущие беременности и роды, какова масса рожденных детей, каким было течение послеродового и послеабортного периодов.
Стенка матки состоит из трех слоев: наружного (серозная оболочка брюшины), мышечного и слизистой оболочки, которая во время беременности претерпевает децидуальные превращения.
В свою очередь в миометрии различают три слоя: наружный, васкулярный и субваскулярный.
Наружный (поверхностный) образован довольно тонким слоем мышечных и соединительнотканных пучков, которые в основном являются продолжением связок: круглых, крестцово-маточных, собственных связок яичников, прямокишечно-маточных и пузырно-маточных. В этот слой вплетаются поверхностные продольные волокна маточных труб. Обращает на себя внимание тесное переплетение связок матки между собой, с мышечными волокнами миометрия правой и левой, передней и задней поверхностей матки.
Продольные и косо расположенные мышцы этого слоя наиболее выражены в дне и теле матки. Большая часть продольных мышц спереди переходит в круглые связки (где они сворачиваются в жгутик), сзади продольные мышцы вплетаются в перешеек и переходят в крестцово-маточные связки. Продольные мышцы влагалища через своды проникают в шейку матки и, переплетаясь с ее циркулярными мышцами, образуют продольный слой шейки (наиболее выраженный по задней поверхности). На рис. 1 видно, как крестцово-маточные (1) и круглые (2) связки вплетаются в продольно расположенные мышечные пучки дна и тела матки, прочно фиксируя матку к костям таза.
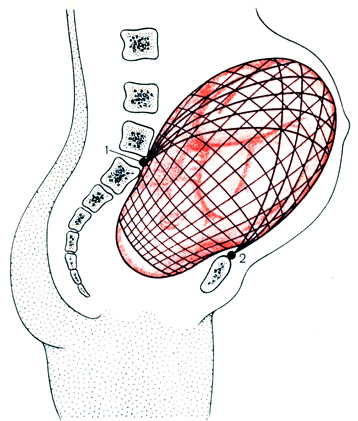
Рис. 1. Беременная матка в сагиттальной проекции (схема). 1 - крестцово-маточные связки; 2 - круглые связки
На рис. 2 также представлен слой матки (упрощенный вариант). Гладкомышечные пучки этого слоя миометрия в дне и теле матки располагаются преимущественно продольно (косопродольно), а в нижнем сегменте и шейке матки - поперечно (циркулярно). Спереди продольные волокна вплетаются в проксимальную часть нижнего сегмента матки, сзади тесно переплетаются со всеми циркулярными волокнами нижнего сегмента и шейки матки. Все связки матки (круглые, пузырно-шеечные, крестцово-маточные, прямокишечно-маточные, кардинальные и широкие) вплетаются не только в наружный, но и срединный слой, прочно фиксируя матку, точнее ее моторный сегмент, к костям таза.
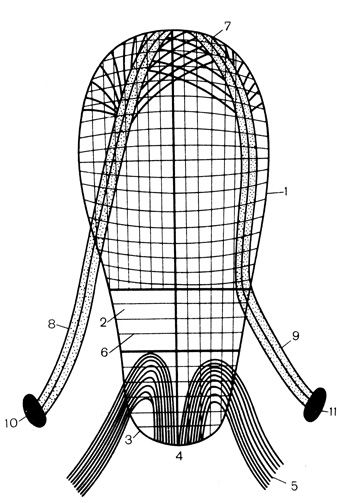
Рис. 2. Срединный (васкулярный) слой миометрия (схема). 1 - тело матки; 2 - перешеек (нижний сегмент); 3 - шейка матки; 4 - влагалище; 5 - продольные мышцы влагалища, вплетающиеся в шейку матки; 6 - циркулярные мышцы перешейка; 7 - ребро матки; 8 - круглые связки; 9 - крестцово-маточные связки; 10 - лонная кость; 11 - крестец
В дне матки основная масса мышечных волокон срединного (васкулярного) слоя миометрия также располагается в продольном направлении, а в нижнем сегменте и шейке матки - поперечно (рис. 2). В нижнем сегменте матки продольные волокна сзади переплетаются с поперечными; спереди в срединном слое миометрия гладкомышечные волокна расположены только в поперечном направлении, в связи с чем возможно тупое разведение мышц матки на передней поверхности нижнего сегмента при кесаревом сечении.
Срединный слой наиболее мощный из всех слоев матки. Продольные мышцы этого слоя наиболее выражены в дне и несколько меньше - в теле матки. Циркулярные мышцы васкулярного слоя в дне матки расположены сравнительно тонким слоем, толщина которого значительно увеличивается в теле и особенно в нижнем сегменте (перешейке), шейке, области внутреннего и наружного зева и стенках влагалища. Помимо этих волокон, существуют циркулярные волокна, оплетающие штопорообразно извитые артерии, расположенные радиально от поверхности матки к ее полости (мышечные спирали). Полагают, что в области шейки наружный и срединный слои очень тонкие [Железнов Б. И., 1973, 1975] или практически отсутствуют [Савицкий Г. А. и др., 1983]. Третий, самый глубокий, слой миометрия - субваскулярный - содержит преимущественно циркулярные мышечные волокна, которые тесно соприкасаются со слизистой оболочкой матки (рис. 3). Пучки мышечных волокон размером около 100 мкм идут по спирали по ходу часовой стрелки. Часть волокон этого слоя имеет обратное направление. В области тела матки волокна перекрещиваются под острым углом, тогда как в нижних отделах, особенно в области шейки, этот угол приближается к тупому. Такое расположение мышечных волокон имеет важное значение в сократительной деятельности матки (СДМ).
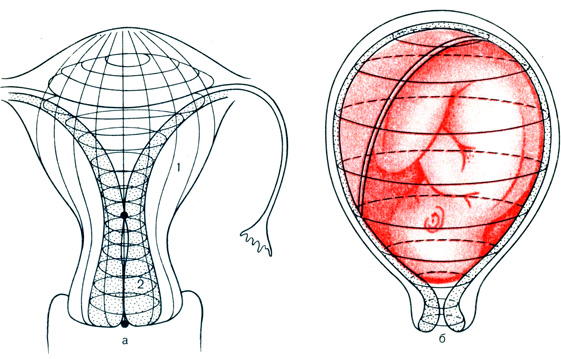
Рис. 3. Наружный и внутренний слой миометрия. а - небеременная матка; б - беременная матка; 1 - наружный слой миометрия в различных отделах небеременной (а) и беременной (б) матки, 2 - внутренний слой
Передняя и задняя стенки матки имеют разное строение. Пучки гладкомышечных волокон спереди соединены более рыхло, вследствие чего передняя стенка матки больше участвует в формировании плодовместилища. Сетчатое переплетение мышечных и соединительнотканных волокон по передней стенке обусловливает ее большую прочность по сравнению с боковыми отделами матки.
При координированных сокращениях матки периоды расслабления мышц глубокого слоя всегда более продолжительные, чем в других слоях. Это приводит к постоянному остаточному увеличению длины мышц и формированию плодовместилища. В родах постоянное активное расслабление этих мышц наряду с непродолжительным и несильным сокращением предохраняет плод от механических воздействий и предотвращает нарушения гемодинамики в субплацентарной зоне миометрия. Из-за отсутствия сокращений этого слоя сохраняется соединение плаценты с маткой в зоне субплацентаоной площадки.
Разное расположение мышечных пучков на передней и задней стенках матки обусловливает большее растяжение передней поверхности тела матки, ее перешейка и надвлагалищной части шейки матки при формировании нижнего сегмента, а также процессы "миграции" низко расположенной плаценты. Задняя стенка матки меньше участвует в формировании плодовместилищ, поэтому при локализации плаценты задней стенки на ее смещение рассчитывать не следует.
I. Daelz (1974) различает два основных функциональных слоя миометрия: наружный, активный, мощный в дне и теле матки, но тонкий, сходящий на нет в дистальном отделе шейки матки, и внутренний, выраженный в шейке и области перешейка, но тонкий в дне и теле матки. Последний слой I. Daelz назвал "зона молчания", подчеркнув его весьма слабую сократительную активность. В родах наружный слой чувствителен к окситоцину, простагландинам и веществам, оказывающим тономоторное действие. Состояние внутреннего слоя в определенной степени отражает функциональную готовность фетоплацентарной системы к родам, которая проявляется в структурных изменениях шейки матки (зрелость шейки матки).
Наличием в матке различных функциональных слоев объясняется особый характер СДМ в родах. Наружный слой активно сокращается и перемещается кверху, а внутренний при этом активно расслабляется, обеспечивая раскрытие шейки матки.
Трансмиссию тяги мышц с тела на шейку матки отрицают Г. А. Савицкий и М. Г. Моряк (1983), которые не обнаружили прямой анатомической связи между мышечными пучками тела и шейки матки. Однако разнообразное расположение ГМК в пучках (параллельно, под углом друг к другу), сложность переплетения их с коллагеновым каркасом, который, с одной стороны, разделяет пучки, а с другой - объединяет в отдельные мышечные комплексы, наличие реципрокности сокращений пучков в зависимости от их расположения и преобладающей иннервации со стороны симпатической или парасимпатической нервной системы позволяют предположить именно перистальтический характер сокращений мышечных пучков в наружном и срединном слоях, что приводит к укорочению и раскрытию шейки матки, а потом к изгнанию плода плаценты.
Однако несомненно, что к началу родов разные отделы матки имеют неодинаковую функциональную активность: наиболее выражена она в дне, теле, нижнем и срединном слоях, тогда как нижний сегмент и субваскулярный слой менее активны. Эти функциональные различия подтверждаются различиями в физиологических и биохимических показателях [Персианинов Л. С., Железнов Б. И., Богоявленская Н. В., 1975; Бакшеев Н. С., Орлов Р. С., 1976], а также неодинаковой реакцией на действие окситоцина, адреналина [Daelz I,1974] и простагландинов [Conrad H. et al., 1974].
Мышечные пучки, элементы соединительной ткани, сосуды и нервы составляют 2/3 массы миометрия. Небольшое содержание гладкомышечных элементов при значительном количестве, соединительной ткани в шейке матки обусловливает ее довольно низкую способность к сокращению. Большое содержание соединительнотканных элементов, в частности коллагеновых волокон, имеет важное значение в механизме укорочения, сглаживания и раскрытия шейки матки в родах. В миометрии гладкомышечные волокна перемежаются с соединительнотканными (коллагеновые и аргирофильные) и эластическими. Содержание мышечной ткани во время беременности увеличивается, при этом наибольшее количество гладкомышечных клеток (ГМК) содержится в дне и теле беременной матки, наименьшее - в дистальном отделе шейки матки (рис. 4).
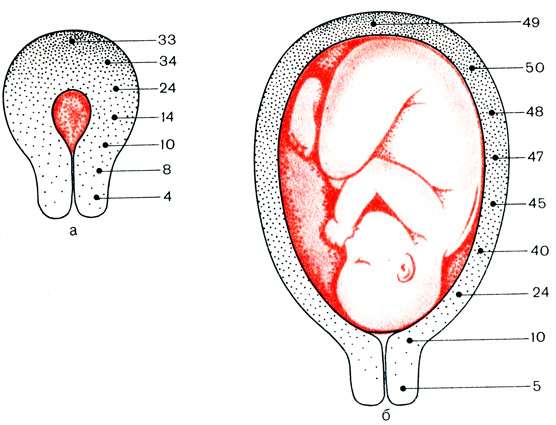
Рис. 4. Процентное содержание мышечных волокон в ткани миометрия в различных отделах небеременной (а) и беременной (б) матки
Между ГМК образуются мостики, по которым возбуждение передается от одной клетки к другой. Однако показано, что возбуждение распространяется также в межклеточных щелевидных пространствах. Большая зона низкого сопротивления обеспечивает синхронизацию сокращений, что обусловливает повышенную возбудимость миометрия и готовность его отвечать сокращением на воздействие медиаторов и веществ, оказывающих тономоторное действие. В ткани миометрия нервный импульс распространяется только на определенное расстояние - "локальная межклеточная регуляция" [Серов В. В., Шехтман А. Б., 1981].
В процессе беременности масса матки увеличивается в среднем с 75 до 1000 г. Объем полости матки возрастает приблизительно в 1000 раз, при этом увеличиваются все размеры матки, в частности продольный размер - с 6 - 7 см вне беременности до 35 - 40 см при доношенной беременности. Увеличиваются также размеры отдельных клеток миометрия: средняя длина - с 50 до 500 - 800 мкм, ширина - с 2 - 4 до 5 - 10 мкм [Mosler K. H., 1968]. Этот феномен является результатом действия гормонов, в частности эстрогенов, а также ответной реакцией матки на длительное растяжение ее растущим плодным яйцом.
Миометрий состоит из сотен биллионов клеток, отдельные мышечные клетки соприкасаются друг с другом примыкающими поверхностями, хотя ограничены контуром клеточной мембраны.
Особенностью гладкомышечной ткани является то, что каждая клетка способна генерировать и распространять потенциалы действия подобно тому, как это наблюдается в скелетных мышцах и сердечной мышце, особенно в элементах системы проводимости миокарда.
Миометрий дна и тела матки состоит в основном из гладкомышечных клеток (лейомиоциты), способных растягиваться, сокращаться, подвергаться гипертрофии и гиперплазии, а после родов возвращаться в исходное состояние.
Особенностью гладкомышечной ткани является также автономность сократительной активности, не подчиняющаяся воле человека. Для гладкомышечной ткани характерно наличие так называемого опорного аппарата, состоящего из коллагеновых и эластических волокон, образующих упругий каркас вокруг каждой ГМК и связывающих пучки мышечных волокон в единый комплекс.
Появлению щелевидных пространств между клетками способствуют эстрогены (фракция эстрадиола - Э2). Способность сокращаться и возвращаться в исходное состояние является главной, но не единственной функцией ГМК, которые способны к активному синтезу коллагена и эластина, регенерации, а также выполняют метаболическую функцию.
На поверхности клеточной мембраны находятся рецепторные белки и гликолипиды, образующиеся под воздействием гормонов. Медиаторная регуляция имеет гуморальный характер. К медиаторам относятся простагландины (ПГ) и циклические нуклеотиды, которые являются модуляторами многочисленных физиологических процессов и патологических реакций, регулируют внутриклеточный обмен и опосредуют действие других факторов (гормоны, биологически активные вещества) на ГМК. Действие их определяет сократительную активность матки.
Сократительная функция матки в родах осуществляется через систему α- и β-адренорецепторов, действие которых определяет возбудимость, тонус, чередование сокращения и расслабления миометрия. α-Адренорецеп- торы вызывают повышение сократительной активности матки, так как реагируют на ПГ, окситоцин, серотонин, гистамин, ацетилхолин, адреналин, норадреналин. Рецепторы этого вида образуются при высоком уровне эстрогенов.
β-Адренорецепторы оказывают противоположное действие на матку: снижают тонус, возбудимость и сократительную активность миометрия. В родах активируются образование и деятельность α-адренорецепции.
Особенности анатомической структуры миометрия имеют большое физиологическое значение, поскольку способствуют распространению возбуждения от одной клетки к другой. Соединительные плазматические отростки являются местом контактирования отдельных клеток друг с другом и областью наименьшего электрического сопротивления, благодаря чему возбуждение распространяется на другие клетки. M. Dewey и K. Barr (1964) назвали эти отростки "несакральные". Важно подчеркнуть, что клетки гладких мышц артерий матки плотно прилегают друг к другу по типу "несакрального" контакта, что указывает на структуральное сходство этих клеток с клетками миометрия.
Импульсы в миометрии распространяются только на определенное расстояние. Электрическое сопротивление при переходе возбуждения с одной клетки на другую является частью сопротивления клеточной мембраны, что облегчает распространение импульсов от одной клетки к другой, от одного пучка мышечных волокон к другому, в результате чего активируются и возбуждаются все мышцы матки. В миометрии отдельные пучки мышечных волокон могут проводить импульсы независимо друг от друга. Скорость проведения импульсов в матке женщин составляет 1 - 5 см/с.
Отдельные участки матки могут обладать различной сократительной активностью, что, вероятно, способствует сохранению определенного тонуса и постоянного внутриматочного давления во время и вне беременности. Только в родах возникают однонаправленные перистальтические сокращения дна, тела и нижнего сегмента матки, обусловливающие процессы раскрытия шейки матки, изгнания плода и плаценты. Каждое возбуждение клетки является источником импульсов возбуждения рядом лежащих клеток, что вызывает волну сокращения распространяющуюся с убывающей силой.
По данным K. Mosler (1968), миометрий имеет следующие особенности по сравнению с миокардом и скелетной мускулатурой: фазы сокращения и расслабления более медленные; время расслабления больше времени сокращения; целостная мышца матки подопытных животных и человека, а также фрагменты миометрия могут сокращаться самостоятельно in vivo и in vitro в течение длительного времени; миометрий относительно долго сохраняет сократительную активность, что, в частности, связано с низким потреблением кислорода; кусочки миометрия могут сохраняться при низкой температуре (4°С), после чего в экспериментальных условиях способны проявлять самостоятельную сократительную активность; автоматической сократительной активностью обладают кусочки миометрия, взятые в любом отделе матки. Все фазы цикла сокращение - расслабление в миометрии протекают в 10 - 20 раз медленнее, чем в миокарде. Этот процесс требует относительно небольших затрат энергии. Автор делает важный вывод, что для усиления сокращения миометрия не следует увеличивать силу сокращения отдельных клеток, достаточно повысить синхронность сокращений отдельных структурных элементов миометрия.
Процесс сокращения в миометрии протекает значительно медленнее, чем в поперечнополосатой мышце, что обусловлено главным образом очень прочными связями между актином и миозином. Кроме того, в связи с более высоким содержанием саркоплазмы в миометрии уменьшается длительность цикла сокращение - расслабление в гладких мышцах.
Матка характеризуется наличием локальной системы ауторегуляции, основанной на межклеточных взаимодействиях. Действие клеточных регуляторов осуществляется по кибернетическим принципам: обратной связи, разнообразия, антагонизма.
Строение и функция гладкомышечной клетки. Основной анатомической структурой миометрия является пучок ГМК, отделенный от других пучков соединительнотканным каркасом. Коллагеновые и эластические волокна, разделяющие пучки мышечных волокон, одновременно связывают группы клеток в единые комплексы. С одной стороны, процесс возбуждения может быстро перейти на ткань миометрия, и тогда волна сокращения (в родах) распространяется со скоростью 5 см/с с убывающей силой. С другой стороны, организованные пучки мышечных волокон могут проводить импульсы независимо друг от друга и отдельные участки, слои, группы пучков миометрия могут сокращаться в различном темпе и с различной амплитудой.
Пучок представляет собой ряд параллельно расположенных ГМК (рис. 5). Соединение клеток в пучках может быть различным. В одних пучках ГМК плотно соприкасаются мембранами, при этом происходит слияние мембран отдельных клеток. Места соединения мембран называют нексусами. В других пучках ГМК расположены под углом друг к другу и соединяются плазматическими мостиками (мостики Проссера). Во время беременности увеличивается количество так называемых шиповидных клеток, которые соприкасаются друг с другом отростками. Не без оснований предполагают, что возбуждение распространяется и в межклеточной среде. У повторнородящих женщин по мере приближения к сроку родов под влиянием эстрогенов увеличивается расстояние между клетками в миометрии, что способствует более быстрому распространению импульса в матке [Орлов Р. С., 1967; Carfield R. E., Hayashi R. H., 1981].
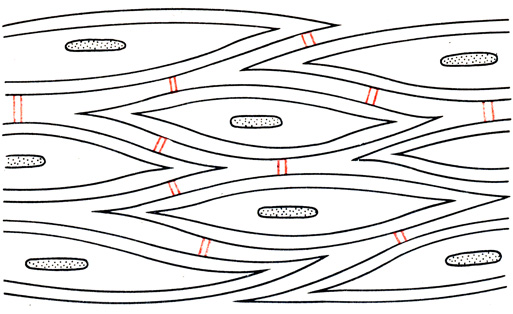
Рис. 5. Строение гладкомышечных клеток в пучке миометрия (схема)
Автоматизм сокращения миометрия, возникающий с началом родовой деятельности, обусловлен не только способностью ГМК вырабатывать импульсы и возможностью генерировать потенциалы действия, но и особым пространственным режимом проведения импульса возбуждения, который обеспечивается системой разнообразных межклеточных и клеточных связей. Эта система имеет важное значение в поддержании гомеостаза при увеличении беременной матки, в процессе родов, когда сокращения и расслабления матки происходят в течение нескольких часов, а иногда и суток, в послеродовом периоде, когда наступает регенерация ГМК [Серов В. В., Шехтер А. Б., 1981]. Таким образом, каждый потенциал действия одной клетки является источником импульса для возбуждения рядом лежащей. Многообразие клеточных контактов в миометрии обусловлено, очевидно, различным функциональным состоянием дна и тела матки по отношению к нижнему сегменту и шейке матки. В то время как одна часть мышечных пучков в каждом слое матки сокращается, другая должна активно расслабляться и растянуться, что способствует сложному перемещению мышечных пучков при формировании плодовместилища во время беременности, сохранению нормального кровотока в матке, растяжению и раскрытию шейки матки, продвижению плода по родовому каналу, отделению и выделению плаценты и уменьшению кровопотери в последовом и раннем послеродовом периодах [Zahn V., 1984].
Форма ГМК веретенообразная, каждая клетка имеет ядро и цитоплазму (саркоплазма) с клеточной оболочкой (сарколемма). Цитоплазма ГМК, помимо органоидов, характерных для клеток всех тканей, имеет сократительный аппарат - миофибриллы, которые располагаются на периферии цитоплазмы и ориентированы вдоль оси клетки. Каждая миофибрилла состоит из пучка тонких нитей (миофиламенты), которые идут от одного конца клетки до другого. Различают тонкие и толстые филаменты. Филамент представляет собой удлиненные молекулы мышечных белков (актиномиозиновые комплексы), занимающие большую часть клетки. ГМК способны к специфическим межклеточным взаимодействиям. С функциональной точки зрения, гладкомышечная ткань характеризуется медленными сокращениями и способностью длительно находиться в состоянии сокращения, затрачивая при этом мало энергии.
Каждая ГМК окружена соединительнотканным ретикулом, состоящим из протофибрилл. Клетка характеризуется выраженной складчатостью, имеет большое количество пиноцитов и отростков, что позволяет ей растягиваться, изменять форму и величину.
Клеточная мембрана состоит из двойного слоя молекул, липидов, к которым с обеих сторон примыкают молекулы белков. В состоянии покоя молекулы липидов расположены таким образом, что их полярные части обращены к белкам, в результате чего создается высокое электрическое сопротивление при низкой ионной проводимости (липидный слой мало проницаем для ионов). Полипептидные цепочки молекул белка располагаются перпендикулярно к молекулам липидов. Белковый слой по структуре напоминает сетку, состоящую из длинных, расположенных параллельно молекул, находящихся на поверхности интерфазы, причем их неполярные группы направлены к неполярной фазе, а полярные - в сторону водной фазы. Клеточная мембрана характеризуется значительной эластичностью и механической резистентностью, которые обусловлены именно наличием белковых слоев, поддерживающих единство ее различных частей. Через клеточную мембрану мышечной клетки легко проходят вещества, растворимые в жирах. Степень проникновения вещества прямо пропорциональна растворимости этого вещества в липидах и обратно пропорциональна размерам его молекул [Ласси Н. И., 1972; Михайленко Е. Т., Чернега М. Я., 1980].
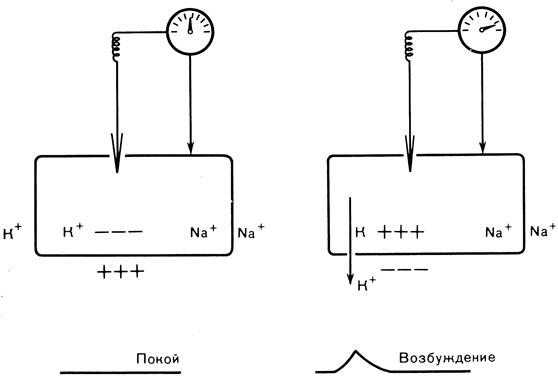
Рис. 6. Схематические изображение потенциала покоя и потенциала действия
Через мембрану в клетку проникают ионы калия и натрия. Они проходят сквозь клеточную мембрану через специальные образования - поры, представляющие собой гидрофильные каналы в клеточной мембране. Эти каналы закрыты, если клетка находится в состоянии покоя. При поступлении импульса поры открываются. Величина пор различна: канальцы для транспорта ионов калия несколько больше, чем для ионов натрия. Движение катионов осуществляется только по выделенным для каждого из них канальцам.
Возбудимость и сократительная активность ГМК зависят от проницаемости ее мембраны для ионов и катионов. Изменение проницаемости (открывание и закрывание пор) происходит под влиянием потенциала покоя или потенциала действия. В состоянии покоя (поляризация мембраны) К+ находятся внутри клетки, Na+ - на наружной поверхности мембраны клетки и в межклеточной среде. При этом на поверхности клетки и в окружающей ее среде создается положительный заряд, а внутри клетки - отрицательный (рис. 6).
При возникновении возбуждения происходят деполяризация клеточной мембраны, которая вызывает потенциал действия (сокращение ГМК). K+, обладая большей проникающей способностью, выходят из клетки, Na+ входят внутрь клетки. При этом сколько K+ вышло из клетки, столько Na+ поступило внутрь клетки (калий-натриевый насос). Каждый ион перемещается по своему канальцу.
Мощным активатором процессов возбуждения, возникновений потенциала действия и сокращения миофибрилл являются ионы кальция (Ca2+). При деполяризации клеточной мембраны Ca2+ поступают внутрь клетки, где захватывают белок тропонин и снимают его блокирующее действие на миофиламенты, при этом актин соединяется с миозином. Ca2+ повышают АТФазную активность актомиозина и поддерживают градиент перемещения K+ и Na+ через клеточную мембрану. Активация проницаемости мембраны для Ca2+ одновременно усиливает и проницаемость ее для Na+. Предполагают, что ионы Na+ и Ca2+ перемещаются через одни канальцы.
В бескальциевой среде механизм сокращения и расслабления ГМК нарушается. В свою очередь ионы Na+, входящие в клетку, конкурируют с ионами Ca2+, частично занимают их место на внутренней мембране. Уменьшение внутриклеточной концентрации Ca2+ и восстановление мембранного потенциала вызывает расслабление ГМК. Часть ионов Ca2+ связывается во внутриклеточных депо, где "складируются", накапливаются до тех пор, пока новый электрический сигнал не высвободит их. Возбуждение клеточной мембраны через систему канальцев приводит к высвобождению кальция из резервуаров. Потенциал действия вновь изменяет физико-химические свойства клеточной мембраны - происходит деполяризация. Благодаря наличию связи клеточной мембраны с саркоплазмой и ядром через саркоплазматическую сеть канальцев синтез РНК усиливается под влиянием эстрогенов, а синтез сократительных белков - под воздействием прогестерона [Wilken H., Heinrich I, Staraube W., 1986].
Кальций накапливается в саркоплазматической сети за счет энергии аденозинтрифосфата (АТФ) по принципу так называемого кальциевого насоса. АТФ необходим как для сокращения, так и для расслабления мышц. Средства, стимулирующие активность α-рецепторов, уменьшают расход кальция, воздействуя на систему аденилциклаза - циклический 3,5-АТФ.
Процесс перемещения ионов зависит от энергии расщепления внутриклеточных субстратов, метаболизма клетки, содержания в межклеточной среде глюкозы, которая является основным энергетическим субстратом для сокращения матки. Сопряженность ионно-транспортных механизмов обусловлена затратой энергии, выделяемой при биохимических процессах в клетке.
Половые гормоны (эстрогены, прогестерон) и биологически активные вещества поддерживают необходимое ионное равновесие и обеспечивают распространение потока электрических зарядов в необходимом направлении (при физиологическом течении беременности и родов сверху вниз, от дна матки к шейке и по горизонтали, захватывая переднюю и заднюю стенки матки). Поток электрических зарядов, который распространяется по мышечному пучку, высвобождает энергию АТФ. Большая часть энергии затрачивается на процесс сокращения мышечного волокна, меньшая - на восстановление клеточной мембраны и запуск ионного насоса.
Диффузия, или проникающая способность ионов, подвержена значительным колебаниям. При проникновении молекул сквозь липопротеидную мембрану возникают энергетические барьеры, которые либо облегчают, либо затрудняют прохождение молекул. Липофильная молекула должна пройти небольшое расстояние от наружного белкового слоя до липидного и от него далее через внутренний слой белка. Гидрофильная молекула легко втягивается белковыми слоями благодаря наличию в них полярных групп, однако наталкивается на барьер в виде неполярных липидов [Hendler R. W., 1975].
При транспорте ионов совершается работа, направленная против электрохимического градиента, для производства которой требуются дополнительные затраты энергии. Активный транспорт ионов является основой сохранения осмотического равновесия в клетке, нормальной концентрации анионов и катионов по обе стороны клеточной мембраны, особенно изнутри, необходимых для ее нормального функционирования. Ионы необходимы как активаторы многочисленных энзиматических реакций, кроме того, они регулируют обмен молекул воды между клеткой и окружающей средой. Выдвинуто несколько гипотез для объяснения механизма активного транспорта ионов через клеточную мембрану. Авторы всех гипотез указывают на темную связь транспорта ионов и других молекул с энергией, вырабатываемой в ходе клеточного метаболизма [Орлов Р. С., Васильев А. Т., 1972; Циркин В. И. и др., 1981].
Очень важными структурными образованиями ГМК являются рибосомы и митохондрии. Рибосомы синтезируют белки и информационные РНК, служащие матрицей для этого синтеза. Митохондрии обусловливают пространственное разделение ферментных систем и являются своеобразной энергетической станцией клетки, где химическая энергия превращается в энергию фосфатных макроэргических связей. Ядро клетки состоит из большого числа сложнейших образований, основными из которых являются ДНК и РНК. Они передают наследственную информацию, генетическую особенность биохимических процессов, осуществляют редупликацию клетки при гиперплазии мышечной ткани.
Отождествлять функции одной ГМК и всего мышечного пучка или слоя миометрия нельзя. Процесс сокращения и расслабления миометрия зависит от расположения пучков по отношению к оси матки (продольное, поперечное, циркулярное, косое и т. д.), характера и плотности адренергических рецепторов (α и β), M- и H-холинорецепторов и других факторов и подчиняются нейрогуморальной регуляции, т. е. значительно сложнее. В субплацентарной зоне и внутреннем слое миометрия, непосредственно прилегающих к полости матки, сохраняется более высокий мембранный потенциал клетки, что не позволяет мышцам этих слоев сильно сокращаться. Благодаря этому плод предохраняется от чрезмерных механических влияний во время родовых схваток и предотвращается преждевременная отслойка плаценты от стенки матки.
При нарушении механизма сокращения мышечного пучка и распространения потока электрических зарядов в миометрии плод в родах может испытывать значительные механические перегрузки, подвергаться "шнурующему" сдавлению циркулярно расположенных мышц, находиться в состоянии гипоксии из-за нарушения маточно-плацентарного кровообращения. У рожениц в этом случае могут возникнуть тяжелые травматические повреждения.
Система сократительных белков миометрия. Различают миофибриллярные, саркоплазматические и строминовые белки миометрия. Миофибриллярные белки обеспечивают сократительную функцию матки, саркоплазматические участвуют в процессе метаболизма ГМК, жировом и углеводном обмене, обеспечивают транспорт кислорода при интенсивной мышечной работе. Строминовые белки относятся к соединительнотканным. Хотя прямого участия в сокращении миометрия они не принимают, но придают упругость и прочность мышечной стенке при ее растяжении. Во время беременности количество всех белков увеличивается, особенно саркоплазматических, которые к сроку родов составляют 40% всех белков миометрия, что значительно усиливает сократительную активность матки.
Мышца матки представляет собой специализированную ткань, обладающую способностью превращать химическую энергию в механическую энергию сокращения. Гладкие мышцы матки содержат следующие миофибриллярные сократительные белки: миозин, актин, тропонин и тропомиозин. Тропомиозин обусловливает тоническую функцию миометрия. При соединении актина с миозином образуется сократительный комплекс - актомиозин, который способен сокращаться (скручиваться). Миозин обладает свойствами АТФазы, а содержащиеся в клетке молекулы АТФ являются источником энергии, необходимой для сокращения. Обладая свойствами фермента, миозин катализирует гидролиз АТФ.
Известно, что миофибриллы состоят из двух видов волокон: толстых и тонких миофиламентов. Толстые волокна образованы в основном из миозина, тонкие - из мономеров актина. Филаменты актина и миозина являются поляризованными.
В покое мостики мышечных клеток выпрямлены благодаря электростатическим силам, действующим между ионизированным АТФ и фиксированным отрицательным зарядом.
Ион кальция, высвобождающийся при возбуждении, образует электрически заряженное звено, связывающее концы мостиков актина и миозина по принципу притяжения. Таким образом, актин и миозин перемещаются с помощью ионов кальция. Одновременно заряды, под действием которых мостики находились в выпрямленном состоянии, нейтрализуются, и мостик сокращается, притягивая нити актина и миозина. Этот цикл повторяется много раз в процессе одиночного сокращения, обусловливая непрерывное движение нитей.
Главным источником энергии в клетке является распад АТФ. Принято считать, что на конце каждой белковой цепочки находится активный энзимный центр, способный разлагать АТФ, а также другой центр, функцией которого является связывание актина. Эти центры, по-видимому, оказывают влияние друг на друга.
Высокой потребностью в энергии во время сокращения матки, особенно в родах, объясняется наличие большого количества гликогена в мышечной клетке, а также обилие митохондрий в саркоплазме между миофибриллами. Миофибриллы идут вдоль всей продольной оси клетки, делясь на саркомеры длиной 2 - 3 мкм каждый. Саркомеры отдельных миофибрилл уложены в правильном порядке рядом друг с другом, в результате чего образуются поперечные полоски, видимые даже в обычном микроскопе.
Скользящий характер мышечного сокращения обусловлен изменениями наклона поперечных мостиков. В процессе сокращения мышцы обязательным является жесткое соединение глобулярной "головы" миозина с актином, а в дальнейшем изменение угла этого соединения в связи с распадом АТФ. H. E. Huxley (1986) и R. Andersson (1973) установили, что силы, действующие между миозином и актином, приводят к скручиванию "головы" миозина тонкого филамента, который затем через посредство другого филамента молекулы миозина действует как прочный, не подвергающийся деформации стержень.
Таким образом, в основе сократительной функции матки лежит процесс превращения химической энергии АТФ в механическую. Сокращение ГМК обусловлено взаимодействием молекул сократительных белков [Бакшеев Н. С., Орлов Р. С., 1976]. При этом основным источником энергии, необходимой для сокращения мышцы, является АТФазная активность миозина. Энергию АТФ использует также актин - второй компонент сократительного белка. Конечным результатом выхода энергии при расщеплении АТФ является скольжение нитей актина и миозина по отношению друг к другу, что приводит к укорочению мышечных клеток, волокон, мышечного пучка, т. е. к сокращению.
Рассмотренные явления свидетельствуют о важности связей между системой сократительных белков и источником энергии, необходимой для сокращения. Вследствие уменьшения потребности в энергии и замедления фаз сократительно цикла миометрий может сокращаться очень длительное время при условии сохранения основного уровня тонуса матки.
При значительном увеличении тонуса миометрия (гипертонус) во много раз увеличиваются расход энергии, распад АТФ и гликогена и в течение нескольких часов наступает истощение энергетических ресурсов матки, схватки резко ослабевают и прекращаются. Существуют две основные причины возникновения этой патологии: некоординированные схватки на фоне гипертонуса миометрия и наличие препятствия для раскрытия шейки или продвижения плода (аномалии развития матки, шейки и матки и влагалища, ригидность маточного зева, низко расположенные миоматозные узлы, узкий таз).
|
ПОИСК:
|
© ROGHDENIEREBENKA.RU, 2010-2019
При копировании материалов активная ссылка обязательна:
http://roghdenierebenka.ru/ 'Беременность, рождение и первые годы жизни ребёнка'
При копировании материалов активная ссылка обязательна:
http://roghdenierebenka.ru/ 'Беременность, рождение и первые годы жизни ребёнка'